17.常温下,下列各组离子在指定溶液中可能大量共存的是( )
| A. | FeCl3溶液中:K+、Na+、SO42-、OH- | |
| B. | 使酚酞试液变红的溶液中:NH4+、Na+、HCO3-、NO3- | |
| C. | 漂白粉溶液中:H+、Na+、I-、Cl- | |
| D. | 与铝反应产生氢气的溶液中:Na+、K+、CO32-、OH- |
16.下列根据实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 浓硫酸与乙醇170℃共热,制得的气体通入酸性KMnO4溶液 | 溶液紫色褪去 | 制得的气体为乙烯 |
| B | 测定等浓度的Na2CO3和Na2SO3的溶液的pH | 前者pH比后者的大 | 非金属性:S>C |
| C | 向2.0ml浓度均为0.1mol•L-1的KCl、KI混合溶液中滴加1~2滴0.01mol•L-1AgNO3溶液,振荡 | 沉淀呈黄色 | Ksp(AgCl)>Ksp(AgI) |
| D | 向待测液中先滴加Ba(NO3)2溶液,再滴加稀盐酸 | 出现白色沉淀 | 原待测液中一定含有SO42- |
| A. | A | B. | B | C. | C | D. | D |
15.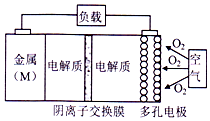 电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
 电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )| A. | “金属(M)〜空气电池”放电过程的正极反应式:O2+2H2O+4e-=4M(OH)n | |
| B. | 比较Mg、Al、Zn三种“金属-空气电池”,“Al-空气电池”的理论比能量最高 | |
| C. | 电解质溶液中的阴离子从负极区移向正极区 | |
| D. | 在“M-空气电池”中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
14.在25℃时,由水电离出的c(H+)为1×10-12mol•L-1,该溶液不可能是( )
| A. | 0.01 mol•L-1的碳酸钠溶液 | B. | pH=12的Ba(OH)2溶液中 | ||
| C. | 0.01 mol•L-1的醋酸 | D. | 0.01 mol•L-1的盐酸 |
13.在101kPa、25℃时,1.0g乙烷气体完全燃烧生成液态水时,放出热量52.0kJ,则乙烷燃烧的热化学方程式为( )
| A. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-1560kJ•mol-1 | |
| B. | 2C2H6(g)+7O2(g)═4CO2(g)+6H2O(g)△H=-1560kJ•mol-1 | |
| C. | C2H6(g)+$\frac{7}{2}$O2(g)═2CO2(g)+3H2O(l)△H=-52.0kJ•mol-1 | |
| D. | 2C2H6(g)+7O2(g)═4CO2(g)+6H2O(l)△H=+3120 kJ•mol-1 |
10.一定条件下,容积为 1L 的密闭容器中发生反应:SiF4(g)+2H2O(g)?SiO2(s)+4HF(g).下列各项中不能说明该反应已达化学平衡状态的是( )
| A. | v(SiF4)消耗=4v(HF)生成 | B. | HF 的体积分数不再变化 | ||
| C. | 容器内气体压强不再变化 | D. | 容器内气体总质量不再变化 |
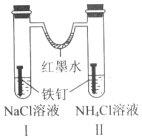
9.如图装置放置一段时间后,铁钉均被腐蚀.下列有关描述不正确的是( )
0 161340 161348 161354 161358 161364 161366 161370 161376 161378 161384 161390 161394 161396 161400 161406 161408 161414 161418 161420 161424 161426 161430 161432 161434 161435 161436 161438 161439 161440 161442 161444 161448 161450 161454 161456 161460 161466 161468 161474 161478 161480 161484 161490 161496 161498 161504 161508 161510 161516 161520 161526 161534 203614

| A. | 红墨水水柱两边的液面变为左低右高 | |
| B. | I 和Ⅱ中负极反应式均为 Fe-2e-=Fe2+ | |
| C. | I 中正极反应式为 O2+2H2O+4e-=4OH | |
| D. | Ⅱ中 NH4Cl 溶液里有气泡产生 |
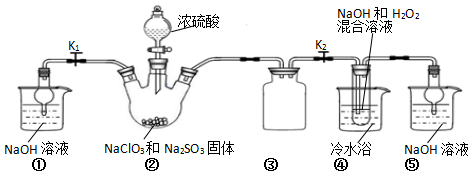 某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究.
某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究.