13.下列物质熔沸点最低的是( )
| A. | 甲烷 | B. | 乙烷 | C. | 丙烷 | D. | 丁烷 |
12.下列事实不能用化学平衡移动原理解释的是( )
| A. | 开启啤酒瓶后,瓶中立刻泛起大量泡沫 | |
| B. | 将盛有二氧化氮和四氧化二氮混合气的密闭容器置于冷水中,混合气体颜色变浅- | |
| C. | 向氯水中加CaCO3后,溶液漂白性增强 | |
| D. | 500℃左右比室温更有利于合成NH3 |
11.在气体反应中,能使反应物中活化分子数和活化分子百分数同时增大的方法是( )
①增大反应物的浓度
②升高温度
③增大压强
④加入催化剂.
①增大反应物的浓度
②升高温度
③增大压强
④加入催化剂.
| A. | ①②③ | B. | ②④ | C. | ②③④ | D. | ①③ |
10.下列说法正确的是( )
| A. | 体积相同,浓度都为 0.1 mol•L-1的盐酸和醋酸分别与体积相同 2 mol•L-1的NaOH溶液反应,两者速率相同 | |
| B. | 用锌和稀硫酸反应制取氢气时,加入少量硫酸铜固体会使生成氢气的速率加快 | |
| C. | Mg粉和Al粉分别与0.1 mol•L-1的NaOH溶液反应,Mg粉反应速率快 | |
| D. | 相同温度下,大理石块与大理石粉分别与盐酸反应,大理石块的反应速率慢 |
8.将一定量的氯气通入30mL浓度为10.00mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断不正确的是( )
| A. | n(Na+):n(Cl-) 可能为7:4 | |
| B. | 与NaOH反应的氯气一定为0.1mol | |
| C. | 若反应中转移的电子为n mol,则0.15<n<0.25 | |
| D. | n(NaCl):n(NaClO):n(NaClO3)可能为11:2:1 |
7.用无机矿物资源生产部分材料,其产品流程示意图如下:下列有关说法正确的是( )
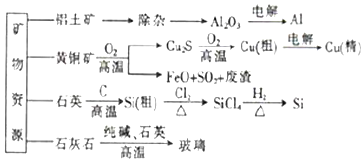

| A. | 制取玻璃和粗硅的同时均产生CO2气体 | |
| B. | 生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应 | |
| C. | 粗硅制高纯硅时,提纯四氯化硅可用过滤的方法(SiCl4的熔点-70℃,沸点57.7℃) | |
| D. | 黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料 |
6.CuSO4溶液中加入过量KI溶液,产生白色CuI沉淀,溶液变棕色.向反应后溶液中通入过量SO2,溶液变成无色.下列说法正确的是( )
| A. | 滴加KI溶液时,CuI是还原产物,KI被还原 | |
| B. | 通入SO2后,溶液变无色,体现SO2的漂白性 | |
| C. | 整个过程发生了复分解反应和氧化还原反应 | |
| D. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 |
5.下列实验过程中产生沉淀的物质的量(Y)与加入试剂的量(X)之间的关系不正确的是( )
0 161311 161319 161325 161329 161335 161337 161341 161347 161349 161355 161361 161365 161367 161371 161377 161379 161385 161389 161391 161395 161397 161401 161403 161405 161406 161407 161409 161410 161411 161413 161415 161419 161421 161425 161427 161431 161437 161439 161445 161449 161451 161455 161461 161467 161469 161475 161479 161481 161487 161491 161497 161505 203614
| A. | 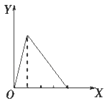 向NaAlO2溶液中滴加稀盐酸至过量且边滴边振荡 | |
| B. | 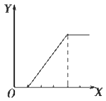 向NaHSO4溶液中逐滴加入KAlO2溶液至过量且边滴边振荡W | |
| C. |  向NH4Al(SO4)2溶液中逐滴加入氢氧化钠溶液直至过量8 | |
| D. | 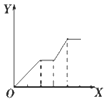 向NaOH、Ba(OH)2、NaA1O2的混合溶液中逐渐通入二氧化碳至过量 |




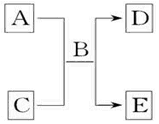 A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系:
A、B、C、D和E均为中学化学常见的纯净物,其中B为自然界中含量最多的液体,它们之间有如图反应关系: