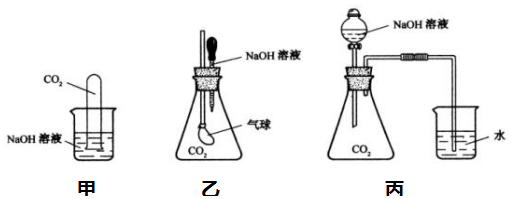
11.下列根据实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向氢氧化镁的饱和溶液中滴加FeCl3溶液,出现红褐色沉淀 | Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| B | 等浓度的Na2CO3和Na2SO3溶液的pH,前者>后者 | 非金属性S>C |
| C | 金属镁片和铝片用灵敏电流计相连,伸入烧碱溶液中,发现镁片上有气泡 | 金属性Mg<A1 |
| D | 冰醋酸中加入水,氢离子浓度先增大,后减小 | 醋酸的电离程度先增大后减小 |
| A. | A | B. | B | C. | C | D. | D |
10.下列实验操作正确的是( )
| A. | 用干燥的PH试纸可以确定某气体是否是氨气 | |
| B. | 在含有FeCl2杂质的FeCl3溶液中通入足量Cl2后,充分加热,可得到纯净的FeCl3溶液 | |
| C. | 中和热测定实验中,碱液要一次性加入,以防止热量损失 | |
| D. | 为减小中和滴定误差,锥形瓶必须用待测液润洗后才能使用 |
9.下列离子方程式书写正确的是( )
| A. | 亚硫酸氢钠的水解:HSO3-+H2O?H3O++SO32- | |
| B. | 甲烷燃料电池(电解质为KOH)负极反应:CH4-8e-+2H2O═CO2+8H+ | |
| C. | 1mol•L-1 NH4A1(SO4)2溶液中逐滴加入等体积4 mol•L-1 NaOH溶液:Al3++4OH-═AlO2-+2H2O | |
| D. | 用硫酸铜溶液去除硫化氢气体Cu2++H2S═CuS↓+2H+ |
8.下列过程或现象与盐类水解无关的是( )
| A. | NaX溶液的pH>7,则可证明HX属于弱电解质 | |
| B. | 二氯化铁溶液可以做电子工业中铜版的刻蚀液 | |
| C. | 实验室盛放NaF溶液不能用玻璃材质的试剂瓶及玻璃塞 | |
| D. | 浓的硫化钠溶液有强烈的臭味 |
7.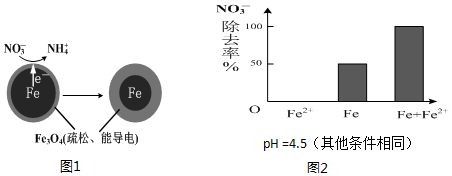 用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.
用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.
(1)Fe还原水体中NO3-的反应原理如图1所示.正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如表:
pH=4.5时,NO3-的去除率低.其原因是FeO(OH)不导电,阻碍电子转移.
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:pH=4.5(其他条件相同)
Ⅰ.Fe2+直接还原NO3-;Ⅱ.Fe2+破坏FeO(OH)氧化层.
①对比实验,结果如图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.
 用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.
用零价铁(Fe)去除水体中的硝酸盐(NO3-)已成为境修复研究的热点之一.(1)Fe还原水体中NO3-的反应原理如图1所示.正极的电极反应式是NO3-+8e-+10H+=NH4++3H2O.
(2)将足量铁粉投入水体中,经24小时测定NO3-的去除率和pH,结果如表:
| 初始pH | pH=2.5 | pH=4.5 |
| NO3-的去除率 | 接近100% | <50% |
| 24小时pH | 接近中性 | 接近中性 |
| 铁的最终物质形态 | 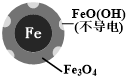 | 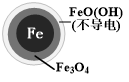 |
(3)实验发现:在初始pH=4.5的水体中投入足量铁粉的同时,补充一定量的Fe2+可以明显提高NO3-的去除率.对Fe2+的作用提出两种假设:pH=4.5(其他条件相同)
Ⅰ.Fe2+直接还原NO3-;Ⅱ.Fe2+破坏FeO(OH)氧化层.
①对比实验,结果如图2所示,可得到的结论是本实验条件下,Fe2+不能直接还原NO3-;在Fe和Fe2+共同作用下能提高NO3-的去除率
②同位素示踪法证实Fe2+能与FeO(OH)反应生成Fe3O4.结合该反应的离子方程式,解释加入Fe2+提高NO3-去除率的原因:Fe2++2FeO(OH)=Fe3O4+2H+,Fe2+将不导电的FeO(OH)转化为可导电的Fe3O4,利于电子转移.
6.下列解释事实的化学方程式或离子方程式,不正确的是( )
| A. | 用FeSO4除去酸性废水中的Cr2O72-:Cr2O72-+6 Fe2++14H+═2Cr3++6 Fe3++7H2O | |
| B. | NH4Al(SO4)2溶液中加入少量的氢氧化钠溶液:Al3++3OH-═Al(OH)3↓ | |
| C. | 用惰性电极电解MgCl2溶液2H2O+2Cl-$\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| D. | 用CaSO4治理盐碱地:CaSO4(s)+Na2CO3(aq)?CaCO3(s)+Na2SO4(aq) |
5.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
0 161304 161312 161318 161322 161328 161330 161334 161340 161342 161348 161354 161358 161360 161364 161370 161372 161378 161382 161384 161388 161390 161394 161396 161398 161399 161400 161402 161403 161404 161406 161408 161412 161414 161418 161420 161424 161430 161432 161438 161442 161444 161448 161454 161460 161462 161468 161472 161474 161480 161484 161490 161498 203614
| A. | 无色透明的溶液:H+、Al3+、NH4+、NO3-、K+ | |
| B. | FeCl3溶液中:K+、Na+、SCN-、Cl- | |
| C. | 能使淀粉KI试纸显蓝色的溶液中:K+、SO42-、S2-、SO32- | |
| D. | 含有0.1 mol•L-1 HCO3-的溶液:Na+、Fe3+、NO3-、SO42- |
 .该反应中氧化剂为HNO3,被还原的元素是N,每生成3.36L标准状况下的气体,转移电子数目为0.45NA(或2.709×1023).
.该反应中氧化剂为HNO3,被还原的元素是N,每生成3.36L标准状况下的气体,转移电子数目为0.45NA(或2.709×1023).