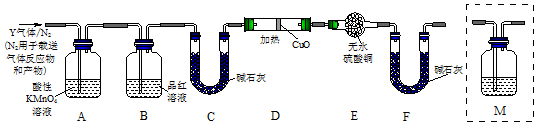
14.下列各组物质中,相互间一定互为同系物的是( )
| A. | C4H10和C20H42 | B. | 邻二甲苯和对二甲苯 | ||
| C. | C4H8O2和C3H6O2 | D. | 一溴乙烷和1,2-二溴乙烷 |
13.下列说法不正确的是( )
①CH3-CH=CH2和CH2=CH2的最简式相同 ②、CH≡CH和C6H6含碳量相同
③丁二烯和丁烯为同系物 ④、正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤在氧气中燃烧只生成二氧化碳和水的有机化合物一定是烃
⑥能够快速、微量、精确的测定相对分子质量的物理方法是核磁共振谱法.
①CH3-CH=CH2和CH2=CH2的最简式相同 ②、CH≡CH和C6H6含碳量相同
③丁二烯和丁烯为同系物 ④、正戊烷、异戊烷、新戊烷的沸点逐渐变低
⑤在氧气中燃烧只生成二氧化碳和水的有机化合物一定是烃
⑥能够快速、微量、精确的测定相对分子质量的物理方法是核磁共振谱法.
| A. | ①和⑤ | B. | ②和③ | C. | ③⑤和⑥ | D. | ④和⑥ |
12.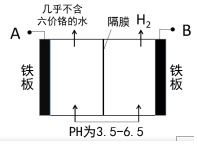 某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,工业设备如图所示,下列说法不正确的是( )
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,工业设备如图所示,下列说法不正确的是( )
 某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,工业设备如图所示,下列说法不正确的是( )
某工厂采用电解法处理含铬废水,耐酸电解槽用铁板作阴、阳极,槽中盛放含铬废水,工业设备如图所示,下列说法不正确的是( )| A. | A接电源正极 | |
| B. | 阳极区溶液中发生的氧化还原反应为:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O | |
| C. | 阴极区附近溶液pH减小 | |
| D. | 若不考虑气体的溶解,当收集到H2 13.44L时(标况),有0.1mol Cr2O72-被还原 |
10.食品的主要成分大都是有机化合物.下列食品中的有机成分不属于高分子化合物的是( )
| A. | 肥肉中的油脂 | B. | 谷类中的淀粉 | C. | 蔬菜中的纤维素 | D. | 瘦肉中的蛋白质 |
8.现代以石油化工为基础的三大合成材料是( )
①塑料 ②合成氨 ③合成盐酸 ④合成橡胶 ⑤合成纤维 ⑥合成尿素 ⑦合成洗涤剂.
①塑料 ②合成氨 ③合成盐酸 ④合成橡胶 ⑤合成纤维 ⑥合成尿素 ⑦合成洗涤剂.
| A. | ②④⑦ | B. | ①②⑦ | C. | ①④⑤ | D. | ②⑥⑦ |
5.下列项目判断,结论正确的是( )
0 161275 161283 161289 161293 161299 161301 161305 161311 161313 161319 161325 161329 161331 161335 161341 161343 161349 161353 161355 161359 161361 161365 161367 161369 161370 161371 161373 161374 161375 161377 161379 161383 161385 161389 161391 161395 161401 161403 161409 161413 161415 161419 161425 161431 161433 161439 161443 161445 161451 161455 161461 161469 203614
| 选项 | 项目 | 结论 |
| A | 三种有机化合物:乙烷、氯乙烯、苯 | 分子内所有原子均在同一平面上 |
| B | C4H8Cl2的同分异构体数目(不考虑立体异构) | 共有10种 |
| C | 乙烯和苯都能使溴水褪色 | 褪色的原理相同 |
| D | 由乙酸和乙醇制乙酸乙酯,油脂水解 | 均属于取代反应 |
| A. | A | B. | B | C. | C | D. | D |
 某化学学习小组利用下列药品和实验装置测定镁铝合金中镁的质量分数.
某化学学习小组利用下列药品和实验装置测定镁铝合金中镁的质量分数.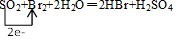 ,
,