14.关于1mol•L-1的硫酸溶液,下列叙述中不正确的是( )
| A. | 1 L该溶液中含溶质98 g | |
| B. | 从10 mL该溶液中取出5 mL后,剩余溶液的浓度为1 mol•L-1 | |
| C. | 将4.9 g浓硫酸加入盛有50 mL蒸馏水的烧杯中,充分溶解后就可配得该浓度的硫酸溶液 | |
| D. | 已知该硫酸为稀硫酸,稀硫酸具有酸的通性,可与锌反应制取氢气 |
13.当足量的Cl2或盐酸分别与下列金属反应时,均有MCl2型化合物生成的是( )
| A. | Fe | B. | Mg | C. | Cu | D. | Ag |
12.在碱性溶液中能大量共存且为无色透明的溶液是( )
| A. | K+、Cl-、MnO4-、SO42- | B. | Na+、K+、NO3-、CO32- | ||
| C. | Na+、NO3-、SO42-、HCO3- | D. | Na+、SO42-、H+、Cl- |
11.为证明醋酸是弱电解质,下列方法不正确的是( )
| A. | 测定0.1mol•L-1醋酸溶液的pH | |
| B. | 测定0.1 mol•L-1CH3COONa溶液的酸碱性 | |
| C. | 比较浓度均为0.1 mol•L-1盐酸和醋酸溶液的导电能力 | |
| D. | 比较相同物质的量浓度的NaOH溶液和醋酸溶液恰好反应完全时消耗两溶液的体积 |
10.下列说法不正确的是( )
| A. | ${\;}_{6}^{14}$C表示质子数为6、中子数为8的核素 | |
| B. | 甲醇(CH3OH)和甘油( 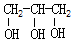 )互为同系物 )互为同系物 | |
| C. | C5H12的同分异构体有3种,其沸点各不相同 | |
| D. | CH3CH2CH2CH(CH3)2的名称是2-甲基戊烷' |
9.下列关于电解法精炼粗铜的叙述中不正确的是( )
| A. | 粗铜板作阳极,纯铜片作阴极,CuSO4溶液作电解液 | |
| B. | 电解时,阳极发生氧化反应,而阴极发生的反应为:Cu2++2e-═Cu | |
| C. | 粗铜中所含Ni、Fe、Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 | |
| D. | 电解铜的纯度可达99.95%~99.98% |
8.工业上常使用电解精炼法将粗铜提纯.在电解精炼铜时( )
| A. | 粗铜接电源负极 | |
| B. | 纯铜作阳极 | |
| C. | 杂质都将以单质形式沉积到池底 | |
| D. | 纯铜片增重2.56 g,电路中通过电子为0.08 mol |
7.
| 物质 | 分子数 | 质量(g) | 物质的量(mol) | 摩尔质量(g•mol-1) |
| N2 | 3.01×1023 | |||
| CO2 | 4.4 | |||
| HCl | 0.5 | |||
| H2SO4 | 49 |
6.相同质量的SO2和SO3它们之间的关系是( )
| A. | 所含硫原子的物质的量之比为1:1 | B. | 氧原子的物质的量之比为3:2 | ||
| C. | 氧元素的质量比为2:3 | D. | 硫元素的质量比为5:4 |
5.若某甲原子(质子数为10)质量是a g,C-12的原子质量是b g,NA是阿伏加德罗常数的值,下列说法正确的是( )
0 161271 161279 161285 161289 161295 161297 161301 161307 161309 161315 161321 161325 161327 161331 161337 161339 161345 161349 161351 161355 161357 161361 161363 161365 161366 161367 161369 161370 161371 161373 161375 161379 161381 161385 161387 161391 161397 161399 161405 161409 161411 161415 161421 161427 161429 161435 161439 161441 161447 161451 161457 161465 203614
| A. | 甲元素的相对原子质量一定是$\frac{12a}{b}$ | |
| B. | 该甲原子的摩尔质量是aNAg | |
| C. | Wg该甲原子的物质的量一定是Wa/(NA)mol | |
| D. | Wg该甲原子所含质子数是10W/a |