15.下列叙述错误的是( )
| A. | 加入肥皂液产生浑浊的水是硬水 | |
| B. | 软水不一定是纯水 | |
| C. | 硬水中的钙、镁离子通过加热煮沸可以完全沉下 | |
| D. | 硬水加入石灰一纯碱后生成Mg(OH)2和CaCO3沉淀;利用离子交换剂也可把硬水软化 |
14.下列过程通电后才能进行的是( )
①电离 ②电解 ③电镀 ④电化学腐蚀.
①电离 ②电解 ③电镀 ④电化学腐蚀.
| A. | ①②③ | B. | ①②④ | C. | ②③ | D. | 全部 |
13.短周期元素W、X、Y、Z在元素周期表中的相对位置如表所示,这四种元素的原子最外层电子数之和为20.则下列说法不正确的是( )
| X | Y | |||
| W | Z |
| A. | 最高价氧化物的水化物的酸性:X<Z | |
| B. | 电负性大小:Y<Z | |
| C. | 离子半径大小:W<Y | |
| D. | W的最高价氧化物的水化物具有两性 |
12.下列有关化学用语正确的是( )
| A. | 氮气分子的结构式N≡N | B. | 钾离子的电子式:K | ||
| C. | 硫原子的结构示意图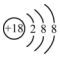 | D. | 二氧化硅的分子式:SiO2 |
11.1.0molPCl3和0.5molCl2充入体积不变的密闭容器中,一定条件下发生下述反应:PCl3(g)+Cl2(g)?PCl5(g);反应达到平衡时,PCl5为0.2mol;如果此时移走0.5molPCl3和0.25molCl2,在相同的温度下再达到平衡时,PCl5的物质的量( )
| A. | 0.2mol | B. | 0.1mol | ||
| C. | 小于0.1mol | D. | 大于0.1mol,小于0.2mol |
10.某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如图所示变化规律(p表示压强,T表示温度,n表示物质的量):根据以上规律判断,下列结论正确的是( )


| A. | 反应Ⅰ:△H>0,p2>p1 | B. | 反应Ⅳ:△H<0,T2>T1 | ||
| C. | 反应Ⅲ:可能是△H>0,T2>T1 | D. | 反应Ⅱ:△H<0,T1<T2 |
9.某温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),发生H2(g)+CO2(g)?CO(g)+H2O(g),其起始浓度如表所示.已知:平衡时甲中CO气体的浓度为0.006mol/L.下列判断不正确的是( )
| 起始浓度(mol/L) | 甲 | 乙 | 丙 |
| C(H2) | 0.010 | 0.020 | 0.020 |
| C(CO2) | 0.010 | 0.010 | 0.020 |
| A. | 反应开始时,丙中的反应速率最快,甲中的反应速率最慢 | |
| B. | 平衡时,甲、乙、丙中CO2的转化率有如下关系:乙>甲=丙=60% | |
| C. | 平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L | |
| D. | 改变条件使乙中温度降低,新平衡中H2的浓度增大,则正反应的△H>0 |
8.常温下,下列说法正确的是( )
| A. | 将pH=5的HCl 溶液稀释1000倍后pH变为8 | |
| B. | 将pH=8的NaOH溶液稀释1000倍后pH变为6 | |
| C. | 将 pH=2的HCl 溶液加热蒸发,体积变为原来的$\frac{1}{10}$,pH变为1 | |
| D. | 将pH=3的醋酸溶液稀释100倍后,pH<5 |
7.下列说法正确的是( )
0 161234 161242 161248 161252 161258 161260 161264 161270 161272 161278 161284 161288 161290 161294 161300 161302 161308 161312 161314 161318 161320 161324 161326 161328 161329 161330 161332 161333 161334 161336 161338 161342 161344 161348 161350 161354 161360 161362 161368 161372 161374 161378 161384 161390 161392 161398 161402 161404 161410 161414 161420 161428 203614
| A. | 冰融化为水的过程△H>0,△S<0 | |
| B. | 在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向 | |
| C. | 在常温下,放热反应一般能自发进行,吸热反应都不能自发进行 | |
| D. | NH4HCO3(s)?NH3(g)+H2O(g)+CO2(g)△H=+185.57kJ/mol,能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向 |