12.已知叠氮酸(HN3)的Ka=10-4.7.下列有关0.1mol•L-1的NaN3溶液中离子浓度的大小关系不正确的是( )
| A. | c(Na+)>c(N3-) | B. | c(N${\;}_{3}^{-}$)>c(OH-) | ||
| C. | c(H+)>c(OH-) | D. | c(Na+)=c(N${\;}_{3}^{-}$)+c(HN3) |
11.固体单质X和气体Y在容积一定的密闭容器中完全反应生成气体Z,相同温度下测得容器内压强不变,若产物气体Z的密度是原气体密度的3倍,则判断正确的是( )
| A. | 反应前后的气体质量之比一定是1:3 | |
| B. | 两种单质X、Y的摩尔质量之比是1:3 | |
| C. | 在生成物Z中,X的质量分数为50% | |
| D. | Z中X、Y两元素的原子个数比为3:1 |
10.下列反应中,熵显著增加的反应是( )
| A. | CO(g)+2H2(g)═CH3OH(g) | B. | CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||
| C. | C(s)+O2(g)═CO2(g) | D. | 2Hg(l)+O2(g)═2HgO(s) |
9.对已经达到衡的下列反应;2X(g)+Y(g)?2Z(g)减小压强时,对反应产生的影响是( )
| A. | 逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 | |
| B. | 逆反应速率减小,正反应速率增大,平衡向正反应方向移动 | |
| C. | 正、逆速率都减小,平衡向逆反应方向移动 | |
| D. | 正、逆速率都增大,平衡向正反应方向移动 |
8.某白色粉末由两种物质组成,为鉴别其组成进行如下实验:①取少量样品加入适量蒸馏水得到澄清溶液;②向①所得的溶液中逐滴加入适量稀硫酸后出现浑浊.该白色粉末不可能是( )
| A. | Al2(SO4)3、NaOH | B. | Al2(NH3)2OH、KOH | C. | BaCl2、NaHCO3 | D. | Ca(ClO)2、NaHSO3 |
7.下列有关表述不正确的是( )
| A. | 向氯水中加入Na2CO3粉末有气体产生 | |
| B. | 用强光照射装满次氯酸的试管(倒置于水槽中)可收集到两种气体 | |
| C. | 漂白粉和次氯酸溶液都是混合物 | |
| D. | 向漂白粉中加入浓盐酸可能产生黄绿色气体 |
6.设NA代表阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 10 mL18.4mol•L-1浓硫酸与足量锌反应,转移电子数为0.184NA | |
| B. | 0.1 mol24Mg18O晶体中所含中子总数为2.0 NA | |
| C. | 在标准状况下,2.8g N2和2.24L CO所含电子数均为1.4NA | |
| D. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的数目为NA |
5.关于铁生锈的机理有人提出如下4步反应:
①Fe(s)-2e-═Fe2+ ②H++e-═H ③4H+O2(g)═2H2O ④4Fe2++O2(g)+(4+2x)H2O═-2(Fe2O3•xH2O)(s)+8H+
根据以上过程,回答下列问题:
(1)根据以上机理,判断下列说法正确的是( )
①Fe(s)-2e-═Fe2+ ②H++e-═H ③4H+O2(g)═2H2O ④4Fe2++O2(g)+(4+2x)H2O═-2(Fe2O3•xH2O)(s)+8H+
根据以上过程,回答下列问题:
(1)根据以上机理,判断下列说法正确的是( )
| A. | 以上锈蚀过程是发生的化学腐蚀 | |
| B. | 从锈蚀反应的最终结果看,水既是氧化剂.又是还原剂 | |
| C. | 反应的实质是氧气被还原,金属铁被氧化 | |
| D. | 从反应机理看,锈蚀过程发生的是析氢腐蚀 |
4.在元素Fe单质及其化合物变化中,下列说法正确的是( )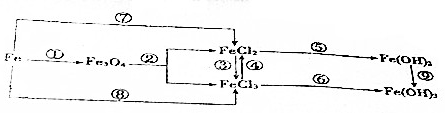
0 161218 161226 161232 161236 161242 161244 161248 161254 161256 161262 161268 161272 161274 161278 161284 161286 161292 161296 161298 161302 161304 161308 161310 161312 161313 161314 161316 161317 161318 161320 161322 161326 161328 161332 161334 161338 161344 161346 161352 161356 161358 161362 161368 161374 161376 161382 161386 161388 161394 161398 161404 161412 203614

| A. | ③反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 钢铁腐蚀时,负极发生的反应是Fe-3e-═Fe3+ | |
| C. | 以Fe为电极,电解饱和NaCl溶液,阳极反应式为2Cl--2e-═Cl2↑ | |
| D. | FeCl2溶液中混有少量FeCl3,可以加入Fe、Cu等金属除去FeCl3 |