19.表是25℃时四种酸的电离平衡常数:
(1)用离子方程式表示NaNO2溶液呈碱性的原因NO2-+H2O?HNO2+OH-
(2)25℃时,向向0.1mol•L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=5
(3)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-
(4)25℃时,等物质的量浓度的HA、NaA混合溶液呈碱性,溶液中各离子浓度的大小顺序为c(Na+)>c(A-)>c(OH-)>c(H+)
(5)已知HNO2不稳定,在稀溶液中也易分解生成NO与NO2,某同学分别取少量NaCl溶液与NaNO2溶液于试管中,分别滴加浓醋酸,以此来鉴别失去标签的NaCl溶液和NaNO2溶液,该方法可行(填“可行”或“不可行”),理由是NaNO2+CH3COOH?CH3COONa+HNO2,2HNO2=H2O+NO+NO2,HNO2不稳定会分解,使平衡不断朝生成亚硝酸的方向移动,可观察到有红棕色气体产生,故此方法可行
(6)已知NaHCO3溶液中存在HCO3??H++CO32-,加水稀释时溶液中的c(H+)将增大(填“增大”或“减小”)
| 化学式 | CH3COOH | HA | HNO2 | H2CO3 |
| Ka | Ka=1.8×10-5 | Ka=4.9×10-10 | Ka=4.6×10-4 | Ka1 =4.1×10-7 Ka2 =5.6×10-11 |
(2)25℃时,向向0.1mol•L-1 CH3COOH溶液中滴加NaOH溶液至c(CH3COOH):c(CH3COO-)=5:9,此时溶液pH=5
(3)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-
(4)25℃时,等物质的量浓度的HA、NaA混合溶液呈碱性,溶液中各离子浓度的大小顺序为c(Na+)>c(A-)>c(OH-)>c(H+)
(5)已知HNO2不稳定,在稀溶液中也易分解生成NO与NO2,某同学分别取少量NaCl溶液与NaNO2溶液于试管中,分别滴加浓醋酸,以此来鉴别失去标签的NaCl溶液和NaNO2溶液,该方法可行(填“可行”或“不可行”),理由是NaNO2+CH3COOH?CH3COONa+HNO2,2HNO2=H2O+NO+NO2,HNO2不稳定会分解,使平衡不断朝生成亚硝酸的方向移动,可观察到有红棕色气体产生,故此方法可行
(6)已知NaHCO3溶液中存在HCO3??H++CO32-,加水稀释时溶液中的c(H+)将增大(填“增大”或“减小”)
18. 煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)SO2分子的空间构型为V形.
(2)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10-3mol•L-1.反应一段时间后溶液中离子浓度的分析结果如表.
①写出NaClO2溶液脱硫过程中主要反应的离子方程式3ClO2-+4NO+4OH-=4NO3-+3Cl-+2H2O.增加压强,SO2的转化率提高(填“提高”“不变”或“降低”).
②随着吸收反应的进行,吸收剂溶液的pH逐渐降低 (填“提高”“不变”或“降低”).
③由实验结果可知,脱硫反应速率大于脱硝反应速率(填“大于”或“小于”).原因是除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高.
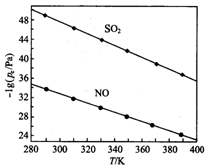
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压Pe如图所示.
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均减小(填“增大”“不变”或“减小”).
②反应ClO2-+2SO32-=2SO42-+Cl-的平衡常数K表达式为$\frac{c(C{l}^{-}){c}^{2}(S{{O}_{4}}^{2-})}{c(Cl{{O}_{2}}^{-}){c}^{2}(S{{O}_{4}}^{2-})}$
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果.从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是形成CaSO4沉淀,降低硫酸根离子浓度,反应平衡向产物方向移动,SO2转化率提高.
 煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:(1)SO2分子的空间构型为V形.
(2)在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10-3mol•L-1.反应一段时间后溶液中离子浓度的分析结果如表.
| 离子 | SO42- | SO32- | NO3- | NO2- | Cl- |
| c/(mol•L-1) | 8.35×10-4 | 6.87×10-6 | 1.5×10-4 | 1.2×10-5 | 3.4×10-3 |
②随着吸收反应的进行,吸收剂溶液的pH逐渐降低 (填“提高”“不变”或“降低”).
③由实验结果可知,脱硫反应速率大于脱硝反应速率(填“大于”或“小于”).原因是除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高.
(3)在不同温度下,NaClO2溶液脱硫、脱硝的反应中,SO2和NO的平衡分压Pe如图所示.
①由图分析可知,反应温度升高,脱硫、脱硝反应的平衡常数均减小(填“增大”“不变”或“减小”).
②反应ClO2-+2SO32-=2SO42-+Cl-的平衡常数K表达式为$\frac{c(C{l}^{-}){c}^{2}(S{{O}_{4}}^{2-})}{c(Cl{{O}_{2}}^{-}){c}^{2}(S{{O}_{4}}^{2-})}$
(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果.从化学平衡原理分析,Ca(ClO)2相比NaClO具有的优点是形成CaSO4沉淀,降低硫酸根离子浓度,反应平衡向产物方向移动,SO2转化率提高.
16. 25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )
25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )
 25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )
25℃时,相同体积和pH的NaX、NaY、NaZ三种盐溶液,分别加水稀释,溶液pH的变化与所加水的体积关系如图所示.下列说法正确是( )| A. | 在上述三种盐原溶液中,水的电离程度大小是NaX>NaY>NaZ | |
| B. | 在等物质的量浓度的NaX、NaY、NaZ混合液中,离子浓度的大小关系是c(Z-)>c(Y-)>c(X-) | |
| C. | 在上述NaX和NaY的混合液中存在$\frac{c(HX)}{c({X}^{-})}$=$\frac{c(HY)}{c({Y}^{-})}$ | |
| D. | 在0.2mol•L-1 NaX溶液中加 入等体积0.1mol•L-1的盐酸,所得混合液中存在c(H+)+c(HX)=c(OH-)+c(Cl-) |
15.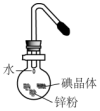 将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )
将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )
 将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )
将碘研碎后与锌粉混合于蒸发皿中,然后滴加少量水,可观察到紫红色蒸气产生,此实验被称为“滴水生烟”.关于该实验的下列说法中错误的是( )| A. | Zn与I2的反应是放热反应 | B. | 水在该反应中作催化剂 | ||
| C. | 生成的碘化锌为紫红色 | D. | 紫红色的蒸气是碘升华所致 |
14.实验室里保存下列试剂的方法,有错误的是( )
| A. | 新制氯水盛放在棕色试剂瓶中,存放于低温避光的地方 | |
| B. | 液溴易挥发,盛放在用水液封、用橡皮胶塞密封的棕色试剂瓶中 | |
| C. | 碘易升华,盛放在棕色试剂瓶中 | |
| D. | 浓盐酸易挥发,盛装在无色密封的细口玻璃试剂瓶中 |
12.有关卤素的说法正确的是( )
| A. | 卤素是典型的非金属元素,其单质只具有氧化性而无还原性 | |
| B. | 卤素单质的熔点随相对分子质量的增大而升高 | |
| C. | 卤化银都不溶于水,也不溶于稍硝酸 | |
| D. | 卤化氢的水溶液都是强酸 |
11.下列说法中正确的是( )
0 161201 161209 161215 161219 161225 161227 161231 161237 161239 161245 161251 161255 161257 161261 161267 161269 161275 161279 161281 161285 161287 161291 161293 161295 161296 161297 161299 161300 161301 161303 161305 161309 161311 161315 161317 161321 161327 161329 161335 161339 161341 161345 161351 161357 161359 161365 161369 161371 161377 161381 161387 161395 203614
| A. | 金属单质在化学反应中只能做还原剂 | |
| B. | 非金属单质在化学反应中只能做氧化剂 | |
| C. | 金属原子在化学反应中失去的电子越多,其还原性就越强 | |
| D. | 置换反应不一定是氧化还原反应 |
 .
.