2.对于化工生产中的化学反应,既要考虑反应的限度和快慢,还要综合考虑成本、设备等因素.
工业制硫酸的重要的一步反应是:2SO2(g)+O2(g)?2SO3(g)△H<0.
(1)在不增加反应物的前提下,从理论上考虑,既能加快反应速率,又能提高SO2转化率的条件是增大压强.
(2)实际生产中的条件是:500℃、催化剂(V2O2),1标准大气压并不断鼓入空气.
①采用500℃的目的是催化剂活性最大.
②用平衡移动原理解释生产过程中不断鼓入空气的目的增大二氧化硫的转化率.
③下表是500℃,不同压强时SO2转化率的变化情况:
请结合表中信息说明采用1标准大气压而不采用更高压强的原因:常压时的转化率较高、高压成本高.
工业制硫酸的重要的一步反应是:2SO2(g)+O2(g)?2SO3(g)△H<0.
(1)在不增加反应物的前提下,从理论上考虑,既能加快反应速率,又能提高SO2转化率的条件是增大压强.
(2)实际生产中的条件是:500℃、催化剂(V2O2),1标准大气压并不断鼓入空气.
①采用500℃的目的是催化剂活性最大.
②用平衡移动原理解释生产过程中不断鼓入空气的目的增大二氧化硫的转化率.
③下表是500℃,不同压强时SO2转化率的变化情况:
| 压强(标准大气压) | 1 | 5 | 10 | 100 |
| SO2转化率(%) | 93.5 | 96.9 | 97.8 | 99.3 |
20.下列配制的溶液浓度偏高的是( )
| A. | 配制盐酸用量筒量取盐酸时俯视刻度线 | |
| B. | 配制盐酸定容时,仰视容量瓶刻度线 | |
| C. | 称量20gNaOH来配制0.5 mol•L-1 NaOH溶液1000 mL 时,砝码错放在左盘 | |
| D. | NaOH溶解后未经冷却即注入容量瓶至刻度线 |
19.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,将22.4L氯化氢溶于足量水中,溶液中含有的HCl分子数为NA | |
| B. | 常温常压下,16gCH4所含中子数目为8NA | |
| C. | 常温常压下,Na2O2与足量H2O反应,共生成0.2molO2,转移电子的数目为0.4NA | |
| D. | 标准状况下,0.1molCl2溶于水,转移的电子数目为0.1NA |
18.NA代表阿伏加德罗常数的值,下列说法错误的是( )
| A. | 2.8g铁与0.05mol Cl2充分反应,转移0.1NA电子 | |
| B. | 27g Al与足量NaOH溶液反应生成 33.6L H2 | |
| C. | 1mol由乙烯(C2H4)和乙烷(C2H6)组成的混合物中含有碳原子的数目为2NA | |
| D. | 0.1mol Na2O2与足量二氧化碳反应转移0.1NA个电子 |
17.同温同压下,A容器中的H2和B容器中的NH3所含氢原子数为3:2,则两个容器的体积比是( )
0 161180 161188 161194 161198 161204 161206 161210 161216 161218 161224 161230 161234 161236 161240 161246 161248 161254 161258 161260 161264 161266 161270 161272 161274 161275 161276 161278 161279 161280 161282 161284 161288 161290 161294 161296 161300 161306 161308 161314 161318 161320 161324 161330 161336 161338 161344 161348 161350 161356 161360 161366 161374 203614
| A. | 3:2 | B. | 1:1 | C. | 9:4 | D. | 1:2 |
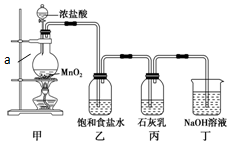 某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.
某兴趣小组设计了下列实验装置探究氯气与石灰乳反应的条件和产物.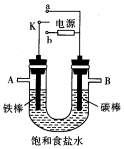 根据如图装置进行电化学的相关实验,回答下列问题.
根据如图装置进行电化学的相关实验,回答下列问题.