15.用固体样品配制一定物质的量浓度的溶液,下列图示对应的有关操作规范的是( )
| A. | 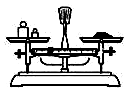 称量 称量 | B. | 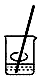 溶解 | C. | 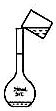 转移 | D. | 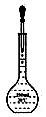 定容 |
14.某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4•7H2O),设计了如图流程:下列说法不正确的是( )
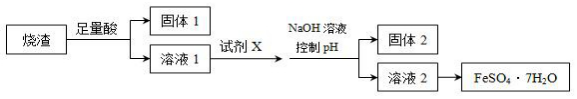

| A. | 溶解烧渣选用足量硫酸,试剂X选用铁粉 | |
| B. | 固体1中一定含有SiO2,控制pH为使Al3+转化为Al(OH)3,进入固体2 | |
| C. | 从溶液2得到FeSO4•7H2O产品的过程中,须控制条件防止其氧化 | |
| D. | 若改变方案,在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4•7H2O |
13.实验需要配制KMnO4溶液,下列操作会引起所配溶液浓度偏大的是( )
| A. | 容量瓶用蒸馏水洗涤后未干燥即用来配制溶液 | |
| B. | 定容时,观察液面俯视刻度线 | |
| C. | 摇匀后,液面低于刻度线,没有再加蒸馏水 | |
| D. | 用蒸馏水洗涤烧杯和玻璃棒.并将洗涤液转移入容量瓶中 |
12.某温度下,H2(g)+CO2(g)??H2O(g)+CO(g)的平衡常数K=$\frac{9}{4}$,该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示,下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol•L-1 | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol•L-1 | 0.010 | 0.010 | 0.020 |
| A. | 平衡时,乙中CO2的转化率大于60% | |
| B. | 平衡时,甲中和丙中H2的转化率均是60% | |
| C. | 平衡时,丙中c(CO2)是甲中的2倍,是0.012 mol•L-1 | |
| D. | 反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
11.合金由于其众多的优点而被航空、航天、航海业广泛关注.下列不属于铝锂合金优点的是( )
| A. | 密度大 | B. | 硬度大 | C. | 抗腐蚀 | D. | 高强度 |
10.根据表提供的数据,判断在等浓度的NaClO、NaHCO3混合溶液中,各种离子浓度关系正确的是( )
| 化学式 | 电离常数 |
| HClO | K1=3×10-8 |
| H2CO3 | K11=4.3×10-7 |
| K12=5.6×10-11 |
| A. | c(HCO3-)>c(ClO-)>c(OH-) | B. | c(ClO-)>c(HCO3-)>c(H+) | ||
| C. | c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3) | D. | c(Na+)+c(H+)=c(ClO-)+c(OH-)+c(HCO3-) |
8.当溶液中X2O72-和SO32-的离子数之比为1:3时正好完全发生氧化还原反应,X在还原产物中的化合价为
( )
( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
7.25℃时,下列各组离子在指定溶液中能大量共存的是( )
0 161177 161185 161191 161195 161201 161203 161207 161213 161215 161221 161227 161231 161233 161237 161243 161245 161251 161255 161257 161261 161263 161267 161269 161271 161272 161273 161275 161276 161277 161279 161281 161285 161287 161291 161293 161297 161303 161305 161311 161315 161317 161321 161327 161333 161335 161341 161345 161347 161353 161357 161363 161371 203614
| A. | 在无色溶液中:Na+、Fe3+、NO3-、Cl- | |
| B. | pH=11的透明溶液中:Na+、K+、MnO4-、CO32- | |
| C. | 在含有HCO3-的溶液中:H+、K+、SO42-、Cl- | |
| D. | 含有大量Fe2+的溶液中:H+、K+、SO42-、NO3- |