6.一定质量的Mg、Al的混合物放入足量的氯气中充分燃烧,固体质量增加7.1g,取等质量的混合物与足量盐酸反应,生成氢气多少( )
| A. | 0.1克 | B. | 0.2克 | C. | 0.3克 | D. | 0.4克 |
5.下列表达式正确的是( )
| A. | S2+的电子式为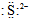 | B. | 碳原子的电子式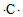 | ||
| C. | 氯原子的结构示意图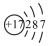 | D. | F-的结构示意图为 |
4.孔雀石的主要成分为Cu2(OH)2CO3,还含少量的FeO、Fe2O3、SiO2.实验室以孔雀石为原料制备CuSO4•5H2O的步骤如图:
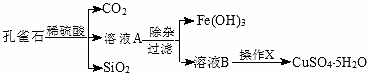
为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如表.请回答:
(1)溶液A中的金属阳离子有Cu2+、Fe2+、Fe3+;若调pH=9.0将杂质铁元素除去,其后果是:Cu2+也会沉淀.
(2)“除杂”时先加入足量H2O2,目的是将Fe2+氧化成Fe3+;再加入CuO固体调节溶液pH的范围至3.2<pH<4.7,其中加入CuO作用是中和溶液中H+使溶液的pH升高,促进Fe3+水解生成Fe(OH)3沉淀(或调节pH至Fe3+的沉淀范围).
(3)操作X包括蒸发浓缩、冷却结晶、过滤和洗涤等;在进行该操作时,将溶液B再适当酸化目的是抑制Cu2+的水解.

为解决有关问题,兴趣小组同学查得有关物质沉淀的pH数据如表.请回答:
| 物质 | pH (开始沉淀) | pH④ (完全沉淀) |
| Fe(OH)3 | 1.9 | 3.2 |
| Fe(OH)2 | 7.0 | 9.0 |
| Cu(OH)2 | 4.7 | 6.7 |
(2)“除杂”时先加入足量H2O2,目的是将Fe2+氧化成Fe3+;再加入CuO固体调节溶液pH的范围至3.2<pH<4.7,其中加入CuO作用是中和溶液中H+使溶液的pH升高,促进Fe3+水解生成Fe(OH)3沉淀(或调节pH至Fe3+的沉淀范围).
(3)操作X包括蒸发浓缩、冷却结晶、过滤和洗涤等;在进行该操作时,将溶液B再适当酸化目的是抑制Cu2+的水解.
1.甲、乙、丙、丁是原子序数依次增大的四种短周期元素,A、B、C、D、E是由其中的两种或三种元素组成的化合物,F是由丙元素形成的单质.已知:A+B=D+F,A+C=E+F;0.1mol•L-1D溶液的pH为13(25℃),下列说法正确的是( )
| A. | 原子半径:丁>丙>乙>甲 | |
| B. | 乙元素在周期表中的位置为第三周期第Ⅳ族 | |
| C. | 1molA与足量B完全反应共转移1mol电子 | |
| D. | 1.0mol•L-1E溶液中阴离子总的物质的量小于0.1mol |
19.将某Fe和Al的混合物m g,加入到足量NaOH溶液中,充分反应后过滤,再将过滤得到的固体加入到足量的CuSO4溶液中,充分反应后过滤得到的固体质量仍为m g,则原混合物中Al的质量分数为( )
| A. | 12.5% | B. | 14.3% | C. | 48.2% | D. | 87.5% |
18.反应2X+3Y═2Z消耗X的质量与生成Z的质量关系如图所示,下列说法正确的是( )
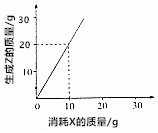

| A. | 有4g Z生成时,则消耗Y 3g | B. | X、Y、Z的摩尔质量之比为1:1:2 | ||
| C. | X、Y、Z的摩尔质量之比为2:3:2 | D. | X、Y、Z的摩尔质量之比为3:2:6 |
17.向50.0mL未知浓度的HCl溶液中加入一定质量分数为20%的AgNO3溶液,充分反应后盐酸有剩余,再向溶液中滴加20g质量分数为20%的NaOH溶液恰好完全反应,则原HCl溶液物质的量浓度是( )
0 161170 161178 161184 161188 161194 161196 161200 161206 161208 161214 161220 161224 161226 161230 161236 161238 161244 161248 161250 161254 161256 161260 161262 161264 161265 161266 161268 161269 161270 161272 161274 161278 161280 161284 161286 161290 161296 161298 161304 161308 161310 161314 161320 161326 161328 161334 161338 161340 161346 161350 161356 161364 203614
| A. | 1.0mol•L-1 | B. | 2.0mol•L-1 | C. | 4.0mol•L-1 | D. | 无法计算 |
 ,COS属于极性分子(填“极性”或“非极性”).
,COS属于极性分子(填“极性”或“非极性”).