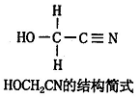
13.一定温度下在一容积不变的密闭容器中发生可逆反应2X(g)?Y(g)+Z(s),以下不能说明该反应达到化学平衡状态的是( )
| A. | 混合气体的密度不再变化 | B. | 反应容器中Y的质量分数不变 | ||
| C. | 体系压强不再变化 | D. | Z的浓度不再变化 |
12.已知H2B在溶液中的电离方程式:H2B=H++HB-,HB-?H++B2-.下列叙述一定正确的是( )
| A. | Na2B溶液存在H2B | |
| B. | NaHB溶液一定显碱性 | |
| C. | NaHB溶液一定显酸性 | |
| D. | NaHB溶液与稀盐酸反应的离子方程式是HB-+H+=H2B |
11.下列说法中正确的是( )
| A. | CuCl2溶液蒸干灼烧后得到CuCl2固体 | |
| B. | 火力发电的目的是使化学能转换为电能 | |
| C. | 已知C(石墨,s)=C(金刚石,s)△H>0,无法比较二者的稳定性. | |
| D. | 将FeCl3固体溶于适量蒸馏水来配制FeCl3溶液 |
9.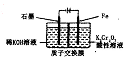 电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )
 电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )
电解法处理酸性含铬废水(主要含有Cr2O72-)时,以铁板作阴、阳极,处理过程中存在反应Cr2O72-+6Fe2+l4H+═2Cr3++6Fe3++7H2O,最后Cr3+以Cr(OH)3形式除去,下列说法不正确的是( )| A. | 阳极反应为Fe-2e-=Fe2+ | |
| B. | 在阴极室,发生的电极反应为:Cr2O72-+6e-+7H2O=Cr(OH)3+8OH- | |
| C. | 在阳极室,pH增大会有Fe(OH)3沉淀生成 | |
| D. | 电路中每转移12 mol电子,最多有1 mol Cr2O72- 被还原 |
8.下列叙述正确的是( )
| A. | NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心 | |
| B. | CH2Cl2是非极性分子,分子中C原子处在H、Cl原子所组成的四边形的中心 | |
| C. | H2O是极性分子.分子中O原子不处在2个H原子所连成的直线的中央 | |
| D. | CO2中的C=O键是极性键,所以CO2是极性分子 |
7.下列有关“核外电子的运动状态”的说法,错误的是( )
| A. | 一个原子轨道就是电子在原子核外的一个空间运动状态 | |
| B. | 电子云表示处于一定空间运动状态电子在核外空间的概率密度分布的描述 | |
| C. | 原子轨道伸展方向与能量大小是无关的 | |
| D. | 除s电子云外,其他空间运动状态的电子云也可以是球形的 |
5.下列叙述正确的是( )
| A. | 0.1mol•L-1氨水中,c(OH-)=c(NH4+) | |
| B. | 在0.1mol•L-1CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) | |
| C. | 10 mL 0.02mol•L-1HCl溶液与10 mL 0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=10 | |
| D. | 0.1mol•L-1某二元弱酸强碱盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
4.下列实验装置、操作能达到实验目的是( )
0 161160 161168 161174 161178 161184 161186 161190 161196 161198 161204 161210 161214 161216 161220 161226 161228 161234 161238 161240 161244 161246 161250 161252 161254 161255 161256 161258 161259 161260 161262 161264 161268 161270 161274 161276 161280 161286 161288 161294 161298 161300 161304 161310 161316 161318 161324 161328 161330 161336 161340 161346 161354 203614
| A. | 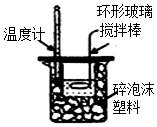 测定中和热 | B. | 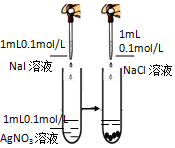 沉淀转化 | ||
| C. | 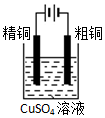 粗铜的电解精炼 | D. | 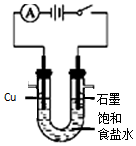 电解食盐水 |
 .
.