3.向a mL0.25mol•L-1的AlCl3溶液中加入金属钠,反应完全后,恰好只形成NaCl和NaAlO2的混合溶液,则加入金属钠的物质的量为( )
| A. | 2.5a×10-4mol | B. | a×10-3mol | C. | 7.5a×10-4mol | D. | a×10-4mol |
2.下列说法中正确的是( )
| A. | 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦 | |
| B. | 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭 | |
| C. | 皮肤上溅有较多的浓硫酸,赶紧用水冲洗 | |
| D. | 衣服沾上大量的浓氢氧化钠溶液,需将此衣服浸泡在盛水的盆中 |
18.某溶液中Cl-、Br-、I-三者物质的量之比为1:2:3,要使溶液中Cl-、Br-、I-物质的量之比为3:2:1,则通入Cl2的物质的量是原溶液中I-的物质的量( )
| A. | $\frac{1}{2}$ | B. | $\frac{1}{3}$ | C. | $\frac{1}{4}$ | D. | $\frac{1}{5}$ |
16.实验室常用氯化铵与氢氧化钙的固体混合加热制取氨气,实验室提供的有关装置见表:
完成下列填空:
(1)从图中选择实验室制取氨气的发生装置b(选填编号)、收集装置①(选填编号).
(2)用注射器收集50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后注射器内无(选填“有”“无”)气体剩余,液体呈红色,用化学方程式解释液体颜色变化的原因NH3+H2O?NH3•H2O?NH4++OH-.
(3)工业合成氨的简易流程如图:
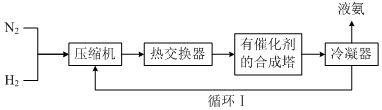
通过循环Ⅰ可利用的气态物质是d
a.催化剂 b.只有N2c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式NaCl+CO2+NH3+H2O→NaHCO3↓+NH4Cl.29NH3、PH3、
AsH3三种氢化物热稳定性由强到弱的顺序是NH3>PH3>AsH3,理由是N、P、As原子半径依次增大,使得N-H、P-H、As-H键长依次增长,热稳定性逐渐减弱.
(5)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4.(NH4)2SO4溶液呈酸性,用离子方程式解释原因NH4++H2O=NH3•H2O+H+;该溶液中存在多种守恒,用离子浓度表示其中一种守恒关系电荷守恒为:[NH4+]+[H+]=2[SO42-]+[OH-]或者物料守恒为:2[SO42-]=[NH4+]+[NH3•H2O].
| 气体发生装置 | 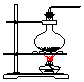 a | 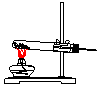 b |  c |
| 气体收集装置 | 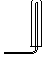 2 | 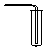 ② | 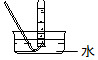 ③ |
(1)从图中选择实验室制取氨气的发生装置b(选填编号)、收集装置①(选填编号).
(2)用注射器收集50mL纯净的氨气,然后再抽取10mL滴有酚酞试液的蒸馏水,并用橡皮塞封闭针头.充分振荡后注射器内无(选填“有”“无”)气体剩余,液体呈红色,用化学方程式解释液体颜色变化的原因NH3+H2O?NH3•H2O?NH4++OH-.
(3)工业合成氨的简易流程如图:

通过循环Ⅰ可利用的气态物质是d
a.催化剂 b.只有N2c.只有H2 d.N2和H2
(4)将 CO2通入到氨化的饱和食盐水中制备NaHCO3固体,反应的化学方程式NaCl+CO2+NH3+H2O→NaHCO3↓+NH4Cl.29NH3、PH3、
AsH3三种氢化物热稳定性由强到弱的顺序是NH3>PH3>AsH3,理由是N、P、As原子半径依次增大,使得N-H、P-H、As-H键长依次增长,热稳定性逐渐减弱.
(5)工业上用氨水吸收SO2尾气,最终得到化肥 (NH4)2SO4.(NH4)2SO4溶液呈酸性,用离子方程式解释原因NH4++H2O=NH3•H2O+H+;该溶液中存在多种守恒,用离子浓度表示其中一种守恒关系电荷守恒为:[NH4+]+[H+]=2[SO42-]+[OH-]或者物料守恒为:2[SO42-]=[NH4+]+[NH3•H2O].
15.硫酸亚铁铵晶体[(NH4)2Fe(SO4)2•6H2O]是一种稳定的还原剂,其制备流程如图1:
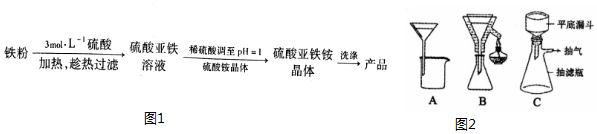
(1)硫酸浓度过大,反应过快同时会使FeSO4溶液中混有Fe3+(填离子符号).
(2)铁粉中混有少量P、S等元素,反应过程中产生的气体有刺激性气味,实验中应采取的措施在通风橱里进行.
(3)铁粉未完全反应,就得趁热过滤,图2中合适的过滤装置是B.
几种物质的溶解度(g/100gH2O)
(4)利用FeSO4与(NH4)2SO4制备(NH4)2Fe(SO4)2•6H2O的原理是由于(NH4)2Fe(SO4)2•6H2O溶解度较小,发生FeSO4+(NH4)2SO4+6H2O=(NH4)2Fe(SO4)2•6H2O,析出晶体(用化学方程式及必要的文字说明).
(5)将(NH4)2SO4晶体加入到FeSO4滤液中,加热搅拌至全部溶解,再蒸发浓缩至溶液表面有晶膜出现时,静置冷却结晶,抽滤,用少量乙醇洗涤晶体2~3次,将晶体放在表面皿上晾干,最终得到的产品质量为19.6g,本次实验产率为77.8%(本次实验使用4.0g铁粉,剩余0.4g未反应).
0 161143 161151 161157 161161 161167 161169 161173 161179 161181 161187 161193 161197 161199 161203 161209 161211 161217 161221 161223 161227 161229 161233 161235 161237 161238 161239 161241 161242 161243 161245 161247 161251 161253 161257 161259 161263 161269 161271 161277 161281 161283 161287 161293 161299 161301 161307 161311 161313 161319 161323 161329 161337 203614

(1)硫酸浓度过大,反应过快同时会使FeSO4溶液中混有Fe3+(填离子符号).
(2)铁粉中混有少量P、S等元素,反应过程中产生的气体有刺激性气味,实验中应采取的措施在通风橱里进行.
(3)铁粉未完全反应,就得趁热过滤,图2中合适的过滤装置是B.
几种物质的溶解度(g/100gH2O)
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 70℃ |
| FeSO4•7H2O | 28.8 | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2SO4 | 70.6 | 73 | 75.4 | 78.0 | 81 | 84.5 | 94.9 |
| (NH4)2SO4•FeSO4•6H2O | 14.5 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(5)将(NH4)2SO4晶体加入到FeSO4滤液中,加热搅拌至全部溶解,再蒸发浓缩至溶液表面有晶膜出现时,静置冷却结晶,抽滤,用少量乙醇洗涤晶体2~3次,将晶体放在表面皿上晾干,最终得到的产品质量为19.6g,本次实验产率为77.8%(本次实验使用4.0g铁粉,剩余0.4g未反应).
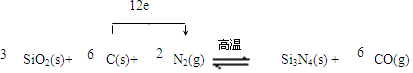 .
.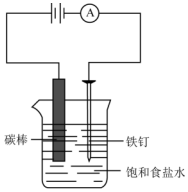 如图所示,回答下列问题:
如图所示,回答下列问题: