11.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,2.24LH2O含有的分子数目为0.1NA | |
| B. | 1mol/LCu(NO3)2溶液中NO3-的数目为2NA | |
| C. | 2.4gMg转变成Mg2+失电子的数目为0.2NA | |
| D. | 6.2gNa2O所含Na+的数目为0.1NA |
10.2016年11月6日中国东北、华北和华东地区爆发空气重度污染,工业排放、机动车排放、冬季燃煤采暖是导致此轮大范围空气重度污染的“元凶”.治理大气污染,任重道远!下列做法与治理大气污染相违背的是( )
| A. | 燃煤电厂的废气随意排放 | |
| B. | 采暖燃煤锅炉安装脱硝等净化设施 | |
| C. | 尽量步行或骑自行车出行 | |
| D. | 重污染工业企业持续推进能源结构调整 |
9.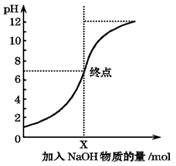 如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )
如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )
 如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )
如图是室温下,向100mL盐酸中逐渐加入NaOH溶液时,溶液的pH变化图象.根据图象所得结论正确的是( )| A. | 原来盐酸的物质的量浓度为0.1mol/L | |
| B. | NaOH溶液的浓度为0.1mol/L | |
| C. | pH=1和pH=7的点对应溶液中水的电离程度相同 | |
| D. | X点NaOH溶液的体积为100mL |
8.下列依据热化学方程式得出的结论正确的是( )
| A. | 已知NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l)△H=-57.3KJ/mol,则40gNaOH固体与稀盐酸完全反应,放出的热量即为57.3KJ | |
| B. | 已知C(s)+O2(g)=CO2(g)△H1 C(s)+$\frac{1}{2}{O_2}$(g)=CO(g)△H2 则△H1<△H2 | |
| C. | 已知H2(g)+Cl2(g)=2HCl,△H=-184.6KJ/mol,则反应物总能量小于生成物总能量 | |
| D. | 已知P(白磷,s)=P(红磷,s)△H<0,则白磷比红磷稳定 |
7.化学与生产、生活息息相关,下列叙述错误的是( )
| A. | 寻找合适催化剂提高合成氨工业中原料的转化率 | |
| B. | 对废旧电池进行回收处理,主要是为了环境保护和变废为宝 | |
| C. | 提高油品质量,可以从一定程度上减少雾霾天气 | |
| D. | 含重金属离子的电镀废液不能随意排放 |
6.表是A、B、C、D、E五种有机物的有关信息:
根据表中信息回答下列问题:
(1)A与溴的四氯化碳溶液反应的生成物的名称为1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学方程式 .
.
(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与KMnO4酸性溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式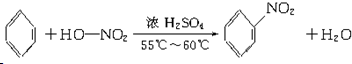 .
.
(4)化合物C的含氧官能团是-OH(写结构),C与E反应能生成相对分子质量为100的酯,该反应类型为酯化反应;其化学方程式为CH3CH2OH+CH2=CHCOOH$?_{△}^{浓H_{2}SO_{4}}$CH2=CHCOOCH2CH3+H2O.
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+H2O.
| A | ①能使溴的四氯化碳溶液褪色; ②能与水在一定条件下反应生成C ③比例模型为: 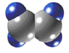 |
| B | ①由C、H两种元素组成; ②球棍模型为: 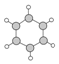 |
| C | ①由C、H、O三种元素组成; ②能与Na反应,但不能与NaOH溶液反应; ③能与E反应生成相对分子质量为100的酯. |
| D | ①相对分子质量比C少2; ②能由C氧化而成; |
| E | ①由C、H、O三种元素组成; ②球棍模型为: 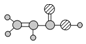 |
(1)A与溴的四氯化碳溶液反应的生成物的名称为1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学方程式
 .
.(2)A与氢气发生加成反应后生成分子F,与F在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
(3)B具有的性质是②③(填序号):①无色无味液体、②有毒、③不溶于水、④密度比水大、⑤与KMnO4酸性溶液和溴水反应褪色、⑥任何条件下不与氢气反应;写出在浓硫酸作用下,B与浓硝酸反应的化学方程式
 .
.(4)化合物C的含氧官能团是-OH(写结构),C与E反应能生成相对分子质量为100的酯,该反应类型为酯化反应;其化学方程式为CH3CH2OH+CH2=CHCOOH$?_{△}^{浓H_{2}SO_{4}}$CH2=CHCOOCH2CH3+H2O.
(5)写出由C氧化生成D的化学方程式2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+H2O.
5.下列有关实验装置及用途叙述完全正确的是( )
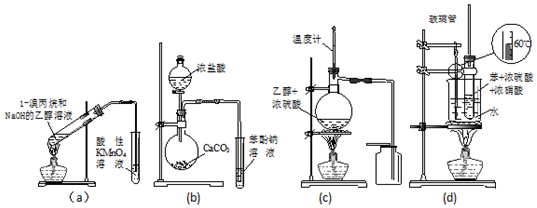

| A. | a装置直接用酸性KMnO4溶液检验消去反应的产物 | |
| B. | b装置检验酸性:盐酸>碳酸>苯酚 | |
| C. | c装置用于实验室制取并收集乙烯 | |
| D. | d装置用于实验室制硝基苯 |
4.NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 标准状况下,11.2L的CHCl3所含的分子数为0.5NA | |
| B. | 17g羟基(-OH)所含有的电子数是10NA | |
| C. | 9.2g甲苯和丙三醇的混合物中,含氢原子数目为0.8NA | |
| D. | 现有乙烯、丙烯的混合气体共28g,其中碳原子数为3NA |
3.1-氯丙烷和2-氯丙烷分别与NaOH乙醇溶液共热的反应,正确的是( )
| A. | 产物不同 | B. | 都属于取代反应 | ||
| C. | 碳氢键断裂的位置相同 | D. | 碳氢键断裂的位置不同 |
2.四氟乙烯(CF2=CF2)是合成聚四氟乙烯(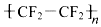 )的材料.
)的材料.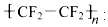 是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )
是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )
0 161116 161124 161130 161134 161140 161142 161146 161152 161154 161160 161166 161170 161172 161176 161182 161184 161190 161194 161196 161200 161202 161206 161208 161210 161211 161212 161214 161215 161216 161218 161220 161224 161226 161230 161232 161236 161242 161244 161250 161254 161256 161260 161266 161272 161274 161280 161284 161286 161292 161296 161302 161310 203614
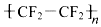 )的材料.
)的材料.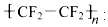 是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )
是不粘锅涂覆物质的主要成分.下列有关说法不正确的是( )| A. | CF2=CF2能使溴的CCl4溶液褪色 | |
| B. | 四氟乙烯合成聚四氟乙烯属于加聚反应 | |
| C. | 1molCF2=CF2只能与1molH2发生加成反应 | |
| D. | 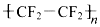 能使高锰酸钾酸性溶液褪色 能使高锰酸钾酸性溶液褪色 |