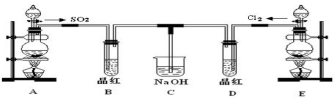
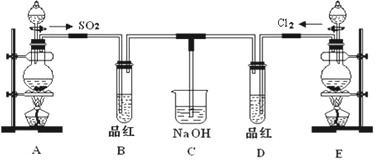
11.设NA为阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,转移4NA个电子 | |
| B. | 标准状况下,22.4 L CCl4中含有CCl4的分子数为NA | |
| C. | 50 mL 12 mol/L盐酸与足量MnO2共热,转移的电子数为0.5NA | |
| D. | 一定条件下,2.3 g Na完全与O2反应生成3.6 g产物时失去的电子数为0.1NA |
10.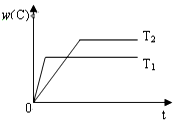 对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )
对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )
 对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )
对于反应A(g)+2B(g)?2C(g),在压强相同的条件下,若生成物C的含量w(C)与时间t的关系如图所示.则下列结论正确的是( )| A. | T1>T2,正反应放热 | B. | T1<T2,正反应放热 | ||
| C. | T1>T2,正反应吸热 | D. | T1<T2,正反应吸热 |
9.如图所示的五种尾气吸收装置中,适合吸收极易溶于水的气体,且能防止产生倒吸现象(溶液进入气体发生装置中)的是( )
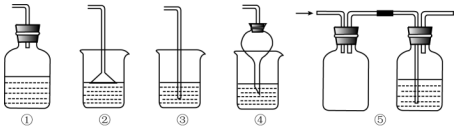

| A. | ②④⑤ | B. | ①②④ | C. | ①②③ | D. | ①②④⑤ |
8.某同学参阅了“84消毒液”说明中的配方,欲用NaClO固体配制480mL含NaClO25%,密度为1.19g/cm3的消毒液.下列说法正确的是( )
| A. | 配制过程只需要三种仪器即可完成 | |
| B. | 容量瓶用蒸馏水洗净后必须烘干才能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液物质的量浓度为3.99mol/L | |
| D. | 需要称量的NaClO固体的质量为140g |
6.汽车尾气无害化处理的反应为2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<O,下列说法不正确的是( )
| A. | 升高温度,活化分子百分数增大,正、逆反应速率都加快 | |
| B. | 使用催化剂,活化分子百分数增大,正、逆反应速率都加快 | |
| C. | 使用催化剂可以降低反应的活化能 | |
| D. | 升高温度,上述反应的平衡常数会增大 |
5.下列有关说法不正确的是( )
| A. | SO42-的空间构型是正四面体形 | |
| B. | CS2分子中各原子均达8电子稳定结构 | |
| C. | 甲醛分子中碳原子的杂化类型为sp2 | |
| D. | CO2与SO2为等电子体 |
4.NA为阿伏加德罗常数,下列叙述中正确的是( )
0 161108 161116 161122 161126 161132 161134 161138 161144 161146 161152 161158 161162 161164 161168 161174 161176 161182 161186 161188 161192 161194 161198 161200 161202 161203 161204 161206 161207 161208 161210 161212 161216 161218 161222 161224 161228 161234 161236 161242 161246 161248 161252 161258 161264 161266 161272 161276 161278 161284 161288 161294 161302 203614
| A. | 0.1 mol NaHSO4晶体中含阴阳离子总数是0.3NA | |
| B. | 将0.1mol FeCl3加到沸水中制得的胶体中,含胶粒0.1NA | |
| C. | 1 mol Na2O2与足量H2O完全反应,转移电子数目为2NA | |
| D. | 在常温常压下,13.8g NO2与足量水充分反应,剩余气体的分子数为0.1NA |