11.一定能在下列溶液中大量共存的离子组是( )
| A. | 含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl- | |
| B. | 含有大量OH-的溶液:Na+、Ca2+、SO42-、CO32- | |
| C. | 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- | |
| D. | 含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
10.阿斯匹林的结构简式为: ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
 ,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )
,则1mol阿斯匹林和足量的NaOH溶液充分反应,消耗NaOH的物质的量为( )| A. | 1mol | B. | 2mol | C. | 3mol | D. | 4mol |
9.下列物质不含官能团的是①(CH3)3C-CH3 ②CH2=CH2 ③CH≡CH ④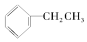 ⑤CH3COOCH3 ⑥
⑤CH3COOCH3 ⑥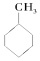
 ⑤CH3COOCH3 ⑥
⑤CH3COOCH3 ⑥
| A. | ②③⑤ | B. | ①⑤⑥ | C. | ①④⑥ | D. | ①④⑤ |
7.X、Y、Z三种元素均位于第三周期,其原子序数逐渐增大,X是本周期原子半径最大的元素,Y的最高价氧化物的水化物与X、Z的最高价氧化物的水化物都能反应,Z的单质是一种黄绿色气体.下列说法不正确的是
( )
( )
| A. | X是第IA元素,Y的最高正价是+3价 | |
| B. | Z是周期表中非金属性最强的元素 | |
| C. | 化合物XZ中含有离子键 | |
| D. | Y的单质与X、Z的最高价氧化物的水化物也都能发生反应 |
6.设 NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 3.9gNa2O2固体中含有的阴离子数为0.05 NA | |
| B. | 标准状况下,2.24LCCl4所含原子数为0.5 NA | |
| C. | 1L 0.1mol/L醋酸溶液中含有的CH3COOH分子数为0.1 NA | |
| D. | 56g铁丝与一定量Cl2发生反应,当铁粉反应完全时,电子转移的数目可能为2.2 NA |
5.下列关于NH4HS溶液的叙述正确的是( )
| A. | 该溶液中,K+、Cu2+、Cl-、ClO-可以大量共存 | |
| B. | 和FeCl3溶液反应的离子方程式:HS-+2Fe3+═S↓+2Fe2++H+ | |
| C. | 和过量NaOH溶液反应的离子方程式:HS-+OH-═S2-+H2O | |
| D. | 向该溶液中通入过量的SO2,无沉淀生成 |
4.有可逆反应Fe(s)+CO2(g)?FeO(s)+CO(g),已知在温度938K时,平衡常数K=1.5,在1173K时,K=2.2,下列叙述正确的是( )
| A. | 该反应达到平衡状态时c(CO2)=c(CO) | |
| B. | 该反应的正反应是放热反应 | |
| C. | 若起始时把Fe和2.0mol CO2放入体积固定为1 L的密闭容器中,某温度时达到平衡,此时容器中CO的浓度为1.0 mol/L,则该温度下上述反应的平衡常数K=1.0 | |
| D. | 若该反应在体积固定的密闭容器中进行,在恒温下达到平衡状态,再通入CO反应混合气体中CO2的物质的量分数增大 |
3.NA为阿伏伽德罗常数的值,下列叙述错误的是( )
| A. | 两份质量均为27 g的 Al分别与足量NaOH溶液和足量的盐酸反应转移电子均为3NA | |
| B. | 1mol氯气与足量的铁反应,转移电子数目是3NA | |
| C. | 46 g NO2和N2O4混合气体中含有原子总数为3 NA | |
| D. | 23 g Na 与足量 O2反应,生成Na2O和Na2O2的混合物,钠失去NA个电子 |
2.下列八种物质:①丙烯、②甲苯、③聚氯乙烯、④乙醇、⑤丙炔、⑥乙酸乙酯、⑦环己烯、⑧溴乙烷中既能使酸性高锰酸钾溶液褪色,又能使溴水因反应而褪色的是( )
0 161106 161114 161120 161124 161130 161132 161136 161142 161144 161150 161156 161160 161162 161166 161172 161174 161180 161184 161186 161190 161192 161196 161198 161200 161201 161202 161204 161205 161206 161208 161210 161214 161216 161220 161222 161226 161232 161234 161240 161244 161246 161250 161256 161262 161264 161270 161274 161276 161282 161286 161292 161300 203614
| A. | ①③④⑤⑦ | B. | ②④⑤⑦ | C. | ④⑤ | D. | ①⑤⑦ |