1.通过粒子散射实验,提出原子结构模型的是( )
| A. | 德谟克利特 | B. | 道尔顿 | C. | 汤姆生 | D. | 卢瑟福 |
20.下列说法错误的是( )
| A. | NaClO溶液中:c(Na+)=c(ClO-)+c(OH-)+c(HClO) | |
| B. | 常温下,pH=a的NH4Cl溶液中由水电离产生的c(OH-)=10-amol•L-1 | |
| C. | 向0.1 mol•L-1的Na2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO32-)均增大 | |
| D. | Na2S稀溶液中:c(OH-)=c(H+)+2c(H2S)+c(HS-) |
19. 已知草酸H2C2O4是二元弱酸.室温下向10mL 0.01mol•L-1 H2C2O4溶液中逐滴加入0.01mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
已知草酸H2C2O4是二元弱酸.室温下向10mL 0.01mol•L-1 H2C2O4溶液中逐滴加入0.01mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
 已知草酸H2C2O4是二元弱酸.室温下向10mL 0.01mol•L-1 H2C2O4溶液中逐滴加入0.01mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )
已知草酸H2C2O4是二元弱酸.室温下向10mL 0.01mol•L-1 H2C2O4溶液中逐滴加入0.01mol•L-1NaOH溶液,其pH变化曲线如图所示(忽略温度变化).下列说法中错误的是( )| A. | a点pH>2 | |
| B. | b点表示的溶液中c(C2O42-)>c(H2C2O4) | |
| C. | c点时加入NaOH溶液的体积为20mL | |
| D. | d点存在c(Na+)+c(H+)=c(OH-)+2c(C2O42-)+c(HC2O4-) |
18.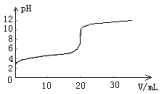 常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
 常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )
常温下,向20.00mL0.1000mol•L-1的醋酸溶液中逐滴加入0.1000mol•L-1的NaOH溶液,pH随NaOH溶液体积的变化如图所示.下列说法不正确的是( )| A. | 在反应过程中,c(Na+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | pH=5时,c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| C. | pH=7时,消耗NaOH溶液的体积肯定小于20.00mL | |
| D. | pH>7时,消耗NaOH溶液的体积肯定大于20.00mL |
17.化学是一门以实验为基础的学科.下列实验操作正确的是( )
| A. | 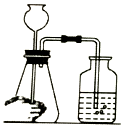 检查装置气密性 | B. | 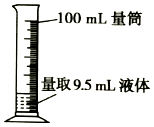 量取 | ||
| C. | 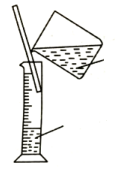 稀释浓硫酸 | D. |  萃取时振荡混合液 |
16.化学在生活中有着广泛的应用,下列对应关系错误的是( )
| 化学性质 | 实际应用 | |
| A. | 三价铁比二价铜氧化性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| B. | 次氯酸盐具有氧化性 | 次氯酸钙可做漂白剂 |
| C. | 稀硝酸可与银反应 | 稀硝酸可除去试管内壁的银镜 |
| D. | HF能与Si反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
| A. | A | B. | B | C. | C | D. | D |
14.已知胆矾溶于水时溶液温度降低,胆矾分解的热化学方程式为:CuSO4•5H2O(S)=CuSO4(S)+5H2O(l)△H=Q1kJ•mol-1;室温下,若将1mol无水硫酸铜溶解为溶液时放热Q2kJ,则下列说法正确的是( )
| A. | Q1>Q2 | B. | Q1=Q2 | C. | Q1<Q2 | D. | 无法比较 |
13.短周期主族元素A、B,C、D的原子序数依次增大.A是周期表中原子半径最小的元素,B是周期期表中能形成化合物最多的元素,C2-和D3+离子的电子层结构相同.下列说法正确的是( )
| A. | 氢化物的稳定:B>C | |
| B. | 简单离子的半径:D>C | |
| C. | 最高氧化物对应的水化物的酸性:B>D | |
| D. | BC2、D2C3中化学键类型相冋 |
12.在一定温度下,将气体 X 和气体 Y 各 0.16mol 充入 10L 恒容密闭容器中,发生反应 X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法正确的是( )
0 161103 161111 161117 161121 161127 161129 161133 161139 161141 161147 161153 161157 161159 161163 161169 161171 161177 161181 161183 161187 161189 161193 161195 161197 161198 161199 161201 161202 161203 161205 161207 161211 161213 161217 161219 161223 161229 161231 161237 161241 161243 161247 161253 161259 161261 161267 161271 161273 161279 161283 161289 161297 203614
| t/min | 2 | 3 | 7 | 9 |
| n(Y)mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前 2 min 的平均速率 v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,反应达到新平衡前 v(逆)>v(正) | |
| C. | 该温度下此反应的平衡常数 K=1.44 | |
| D. | 其他条件不变,再充入 0.2 mol Z,平衡时 X 的体积分数增大 |