1.在给定的条件下,下列物质间的转化均能实现的是( )
| A. | NH3$→_{催化剂}^{O_{2}}$NO$\stackrel{NaOH溶液}{→}$NaNO3 | |
| B. | Fe2O3$→_{高温}^{Al}$Fe$→_{点燃}^{Cl_{2}}$FeCl3 | |
| C. | SiO2$→_{△}^{H_{2}O}$H2SiO3$\stackrel{NaOH溶液}{→}$NaSiO3 | |
| D. | NaSO4溶液$\stackrel{BaCl_{2}溶液}{→}$BaSO4$\stackrel{盐酸}{→}$BaCl2 |
20.下列陈述I、陈述II正确并且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | HC1O具有漂白性 | 湿润的Cl2能使有色布条褪色 |
| B | SiO2具有导电性 | SiO2可用于制光导纤维 |
| C | 铝的金属性比铁强 | 铝制品在空气中比铁制品更容易腐蚀 |
| D | 碳酸钠属于碱类 | 工业上的“三酸二碱”,把碳酸钠归纳为“碱” |
| A. | A | B. | B | C. | C | D. | D |
19.用NA表示阿伏加徳罗常数的数值,下列判断正确的是( )
| A. | 常温常压下,22.4 L CO2含有的分子数为NA | |
| B. | 1mol•L-1的Ba(OH)2溶液中含有的氢氧根离子数目为2NA | |
| C. | 常温常压下,18 g H2O含有的氢原子数为2NA | |
| D. | 1mol Fe在足量的Cl2中充分燃烧,转移的电子数为2NA |
18.下列有关物质的性质或用途的叙述中不正确的是( )
| A. | 碳酸氢钠可用于治疗胃酸过多 | |
| B. | 用氯化钡溶液可鉴别SO42-和CO32- | |
| C. | CO、NO、NO2都是大气污染物 | |
| D. | 常温下,可用铝制或铁制槽车运输浓硫酸 |
16.NA表示阿伏伽德罗常数的值,下列叙述不正确的是( )
| A. | 标准状况下22.4L水含有的分子数为NA | |
| B. | 0.5mol氢气中氢原子数为6NA | |
| C. | 常温下5.6g铁与足量盐酸反应失去的电子数为0.2NA | |
| D. | 标准状况下22.4LCO2与CO的混合气体含分子数为NA |
15.下列事实与胶体无关的是( )
| A. | 大海中航标灯形成的光射线 | B. | 二氧化碳产生的温室效应 | ||
| C. | 长江入海口形成三角洲 | D. | 工矿排放的烟尘遇空气形成雾霾 |
14.二氧化碳的回收利用是环保领域研究热点.
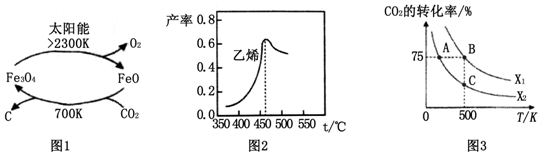
(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如图1所示.总反应的化学方程式为CO2$\frac{\underline{\;太阳能\;}}{FeO}$C+O2.
(2)在催化剂M的作用下,CO2和H2同时发生下列两个反应:
a.2CO2(g)+6H2(g)?CH2=CH2(g)+4H2O(g)△H<0
b.2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H<0
图2是乙烯在相同时间内,不同温度下的产率,则高于460℃时乙烯产率降低的原因可能是AC(填序号).
A.催化剂M的活性降低B.a反应的平衡常数变大
C.生成甲醚的量增加 D.b反应的活化能增大
(3)CO2经过催化氢化合成乙烯反应为:2CO2(g)+6H2(g)?CH2=CH2(g)+4H2O(g)△H<0
在密闭容器中充入2mol CO2和nmol,在一定条件下发生反应,CO2的转化率与温度、投料比X=[$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图3所示.
①投料比X1>X2(填“>”、“<”或“=”下同),平衡常数KA、KB、KC的大小关系为KA>KB=KC;
②TK时,某密闭容器发生上述反应,反应进行到不同时间测得各物质的浓度如表:
20~30min间只改变了某一条件,根据表中的数据判断改变的条件可能是缩小容器体积.该温度下0~10min内H2的反应速率为0.06mol•L-1•min-1.

(1)在太阳能的作用下,以CO2为原料制取炭黑的流程如图1所示.总反应的化学方程式为CO2$\frac{\underline{\;太阳能\;}}{FeO}$C+O2.
(2)在催化剂M的作用下,CO2和H2同时发生下列两个反应:
a.2CO2(g)+6H2(g)?CH2=CH2(g)+4H2O(g)△H<0
b.2CO2(g)+6H2(g)?CH3OCH3(g)+3H2O(g)△H<0
图2是乙烯在相同时间内,不同温度下的产率,则高于460℃时乙烯产率降低的原因可能是AC(填序号).
A.催化剂M的活性降低B.a反应的平衡常数变大
C.生成甲醚的量增加 D.b反应的活化能增大
(3)CO2经过催化氢化合成乙烯反应为:2CO2(g)+6H2(g)?CH2=CH2(g)+4H2O(g)△H<0
在密闭容器中充入2mol CO2和nmol,在一定条件下发生反应,CO2的转化率与温度、投料比X=[$\frac{n({H}_{2})}{n(C{O}_{2})}$]的关系如图3所示.
①投料比X1>X2(填“>”、“<”或“=”下同),平衡常数KA、KB、KC的大小关系为KA>KB=KC;
②TK时,某密闭容器发生上述反应,反应进行到不同时间测得各物质的浓度如表:
| 时间/min 浓度/mol•L-1 | 0 | 10 | 20 | 30 | 40 | 50 |
| H2(g) | 6.00 | 5.40 | 5.10 | 9.00 | 8.40 | 8.40 |
| CO2(g) | 2.00 | 1.80 | 1.70 | 3.00 | 2.80 | 2.80 |
| CH2=CH2(g) | 0 | 0.10 | 0.15 | 0.50 | 0.60 | 0.60 |
13.下列有关物质的性质与其应用相对应的是( )
0 161093 161101 161107 161111 161117 161119 161123 161129 161131 161137 161143 161147 161149 161153 161159 161161 161167 161171 161173 161177 161179 161183 161185 161187 161188 161189 161191 161192 161193 161195 161197 161201 161203 161207 161209 161213 161219 161221 161227 161231 161233 161237 161243 161249 161251 161257 161261 161263 161269 161273 161279 161287 203614
| A. | 铝热反应可以快速制取单质铁,工业上常用此法冶炼铁 | |
| B. | NaHCO3能与碱反应,食品工业中用做焙制糕点的膨松剂 | |
| C. | K2FeO4具有强氧化性,其产物水解生成Fe(OH)3胶体,故可用于自来水消毒和净化 | |
| D. | SO2具有漂白性,可用于食品的消毒和漂白 |
 向一容积为5L的恒容密闭容器内,充入0.2mol CO和0.4mol H2O,在一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H>0.反应中CO2的浓度(c) 随时间(t)的变化关系如图所示.
向一容积为5L的恒容密闭容器内,充入0.2mol CO和0.4mol H2O,在一定条件下发生反应:CO(g)+H2O(g)?CO2(g)+H2 (g)△H>0.反应中CO2的浓度(c) 随时间(t)的变化关系如图所示.