8.在某恒温、恒容的密闭容器内发生反应:2NO2(g)?2NO(g)+O2(g)△H>0,开始时充入2molNO2并达到平衡,下列说法正确的是( )
| A. | 再充入2molNO2,平衡正向移动,O2的体积分数增大 | |
| B. | 升高温度,O2的体积分数减小 | |
| C. | 充入N2,平衡不移动 | |
| D. | 再充入1molO2,NO2的体积分数增大 |
7.某温度下,对可逆反应:2X(g)+Y(g)?Z(g)+W(s)△H>0,则下列叙述正确的是( )
| A. | 加入少量W,逆反应速率增大 | |
| B. | 升高温度时,正反应速率增大,逆反应速率减小 | |
| C. | 压强不变,充入与反应体系不反应的N2,Z的物质的量减少 | |
| D. | 平衡后加入X,上述反应的△H增大 |
6.某澄清溶液可能由KI、NaNO3、CaCl2和Na2CO3中的一种或几种混合而成,为鉴定其组成,依次进行如下实验;(1)上述溶液中滴加AgNO3溶液有浅黄色沉淀产生;(2)将沉淀滤出加HNO3时,沉淀部分溶解,有气体放出;(3)向一份溶液中加淀粉溶液,再加适量氯水,溶液显蓝色.根据以上实验可判断( )
| A. | 一定有CaCl2和Na2CO3,一定没有KI,可能有NaNO3 | |
| B. | 一定有KI、Na2CO3,可能有NaNO3、CaCl2 | |
| C. | 一定有KI、Na2CO3,可能有NaNO3,一定没有CaCl2 | |
| D. | 只有Na2CO3,可能有NaNO3,一定没有KI、CaCl2 |
5.一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的( )
①NaOH(固体)
②NaCl溶液
③HCl
④CH3COONa(固体)
①NaOH(固体)
②NaCl溶液
③HCl
④CH3COONa(固体)
| A. | ①② | B. | ②③ | C. | ③④ | D. | ②④ |
2.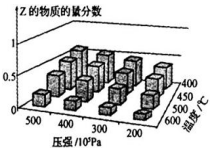 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
( )
 为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是
为探究外界条件对反应:mA(g)+nB(g)?cZ(g)△H 的影响,以A和B物质的量之比为m:n开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示.下列判断正确的是( )
| A. | 在恒温恒压条件下,向已达到平衡的体系中加入少量Z,达新平 衡时,Z的物质的量分数不变 | |
| B. | 升高温度,正、逆反应速率都增大,平衡常数增大 | |
| C. | △H>0,m+n>c | |
| D. | 温度不变,增大压强,平衡正向移动,达新平衡时,A的浓度比原平衡减小 |
1.下列说法正确的是( )
| A. | 破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量,该反应为吸热反应 | |
| B. | 任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同 | |
| C. | 已知:①2H2(g)+O2(g)=2H2O(g)△H1,②2H2(g)+O2 (g)=2H2O(1)△H2,则△H1<△H2 | |
| D. | 已知:①C(s,石墨)+O2 (g)=CO2(g)△H=-393.5kJ•mol-1, ②C(s,金刚石)+O2(g)=CO2 (g)△H=-395.0 kJ•mol-1则C(s,石墨)=C(s,金刚石)△H=+1.5 kJ•mol-1 |
20.下列过程或现象与盐类水解无关的是( )
0 161047 161055 161061 161065 161071 161073 161077 161083 161085 161091 161097 161101 161103 161107 161113 161115 161121 161125 161127 161131 161133 161137 161139 161141 161142 161143 161145 161146 161147 161149 161151 161155 161157 161161 161163 161167 161173 161175 161181 161185 161187 161191 161197 161203 161205 161211 161215 161217 161223 161227 161233 161241 203614
| A. | 热的纯碱溶液去油污效果比冷的纯碱溶液去油污效果好 | |
| B. | 加热稀醋酸溶液其pH 稍有减小 | |
| C. | 实验室制FeCl3溶液时,把FeCl3固体溶于浓盐酸中,再加水稀释到所需的浓度 | |
| D. | 草木灰与铵态氮肥不能混合使用 |
