3.氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等.下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
| A. | 3NO2+H2O→2HNO3+NO | B. | 4Fe(OH)2+O2+2H2O→4Fe(OH)3 | ||
| C. | 2F2+2H2O→4HF+O2 | D. | 2H2O$\stackrel{通电}{→}$O2+2H2↑ |
2.下列叙述正确的是( )
| A. | 若AgCl沉淀完全,就是指氯化银溶液中溶质离子的浓度为零 | |
| B. | 达到溶解平衡时,晶体就不再溶解 | |
| C. | 室温下,在100g水中能溶解1~10g的溶质,这种物质被称为可溶性物质 | |
| D. | 无机酸都是可溶的 |
1.以下变化明显吸热的是( )
| A. | 盐酸与NaOH溶液混合 | B. | 固体NaCl加入水中 | ||
| C. | 固体NH4Cl加入水中 | D. | 固体CaO加入水中 |
20.鉴别Cl-、Br-、I-可以选用的试剂是( )
| A. | 溴化钠溶液与四氯化碳 | B. | 碘化钾淀粉溶液 | ||
| C. | 氯水、四氯化碳 | D. | 碘水、淀粉溶液 |
19.白磷分子如图所示:则31g白磷中存在的共价键数目为( )
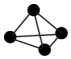

| A. | 4NA | B. | NA | C. | 1.5NA | D. | 0.25NA |
18.下列原子中可以形成R+离子的是( )
| A. | 核电荷数为13 | B. | 质子数为17 | ||
| C. | M层比L层少6 | D. | 质量数为23,中子数为12 |
17.根据下列能量变化示意图,分析下列说法中正确的是( )


| A. | A(g)+B(g)→C(g)+D(l)是放热反应 | |
| B. | A(g)+B(g)→C(g)+D(l)是吸热反应 | |
| C. | C(g)+D(l)→A(g)+B(g)是放热反应 | |
| D. | C(g)+D(l)具有的能量大于A(g)+B(g)具有的能量 |
16.新鲜水果中富含维生素C,可用碘测定其含量.其原理为:维生素C+I2→脱氢维生素C+HI.在该反应中,氧化剂及其还原产物是( )
| A. | 维生素C和脱氢维生素C | B. | 维生素C和HI | ||
| C. | I2和HI | D. | I2和脱氢维生素C |
15.下列物质的电子式或结构式书写正确的是( )
| A. | 氯化铵的电子式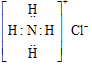 | B. | 氮气的电子式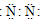 | ||
| C. | 次氯酸的结构式H-Cl-O | D. | 氯化钙的电子式 |
14.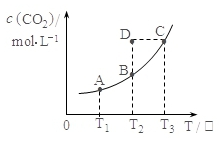 在密闭容器中存在下列平衡:CO(g)+H 2O(g)?CO2(g)+H 2(g);CO 2(g)的平衡物质的量浓度c(CO 2)与温度T的关系如图所示.下列说法错误的是( )
在密闭容器中存在下列平衡:CO(g)+H 2O(g)?CO2(g)+H 2(g);CO 2(g)的平衡物质的量浓度c(CO 2)与温度T的关系如图所示.下列说法错误的是( )
0 161030 161038 161044 161048 161054 161056 161060 161066 161068 161074 161080 161084 161086 161090 161096 161098 161104 161108 161110 161114 161116 161120 161122 161124 161125 161126 161128 161129 161130 161132 161134 161138 161140 161144 161146 161150 161156 161158 161164 161168 161170 161174 161180 161186 161188 161194 161198 161200 161206 161210 161216 161224 203614
 在密闭容器中存在下列平衡:CO(g)+H 2O(g)?CO2(g)+H 2(g);CO 2(g)的平衡物质的量浓度c(CO 2)与温度T的关系如图所示.下列说法错误的是( )
在密闭容器中存在下列平衡:CO(g)+H 2O(g)?CO2(g)+H 2(g);CO 2(g)的平衡物质的量浓度c(CO 2)与温度T的关系如图所示.下列说法错误的是( )| A. | 平衡状态A与C相比,平衡状态A的c(CO)小 | |
| B. | 在T 2时,若反应处于状态D,则一定有V 正<V 逆 | |
| C. | 反应CO(g)+H 2O(g)?CO 2(g)+H 2(g) 的△H>0 | |
| D. | 若T 1、T 2时的平衡常数分别为K 1、K 2,则K 1<K 2 |