1.容量瓶上不需要标注的项目是( )
| A. | 温度 | B. | 容量 | C. | 浓度 | D. | 刻度线 |
20.下列说法正确的是( )
| A. | 氧气的气体摩尔体积是22.4L | B. | 硫酸的摩尔质量是98g | ||
| C. | CO2的相对分子质量是44g | D. | CO32-摩尔质量是60g/mol |
19.若50滴水正好是m mL,则1滴水所含的分子数是( )
| A. | m×50×18×6.02×1023 | B. | $\frac{m×6.02×1{0}^{23}}{50×18}$ | ||
| C. | $\frac{18m×6.02×1{0}^{23}}{50}$ | D. | $\frac{50×18×m}{6.02×1{0}^{23}}$ |
18.室温下,向100mL 0.1mol/L的H2SO4中加入足量的锌粒,若想减慢制取H2的速率,但又不影响H2的体积,向硫酸溶液中加入试剂可以选( )
①硝酸钠溶液 ②醋酸钠溶液③碳酸钠溶液 ④氯化钠溶液.
①硝酸钠溶液 ②醋酸钠溶液③碳酸钠溶液 ④氯化钠溶液.
| A. | ①② | B. | ②④ | C. | ③④ | D. | ①③ |
17.如图为某种甲醇燃料电池示意图,工作是电子流动方向如图所示,下列判断正确的是( )
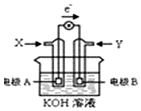

| A. | X位氧气 | |
| B. | 电极材料活泼性为:A>B | |
| C. | 电极B附近溶液碱性增强 | |
| D. | 电极A的反应式:CH3OH-6e-+H2O═CO2+6H+ |
16.设NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 标准状况下,22.4LSO3含有的分子数为NA | |
| B. | 常温常压下,7.8gNa2O2含有的阴离子数目为0.2NA | |
| C. | 将含lmol FeCl3的溶液制得的Fe(OH)3胶体中含胶粒数为NA(假设所有的FeCl3都转化为Fe(OH)3胶体) | |
| D. | 在反应KIO3+6HI=KI+3I2+3H2O中,每生成3molI2转移的电子数为5NA |
15.下列有关实验操作说法中,正确的是( )
| A. | 用托盘天平称取5.85gNaCl | |
| B. | 用广泛pH试纸测得橙汁pH为3.50 | |
| C. | 用酸式滴定管量取25.00 mL高锰酸钾溶液 | |
| D. | 用酸性高锰酸钾溶液检验FeCl3中是否含有FeC12 |
14.NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 60克SiO2含有2NA个Si-O共价键 | |
| B. | 实验室中用含4molHCl的浓盐酸跟足量MnO2加热反应可制得Cl2的分子数为NA | |
| C. | 1L 0.2mol•L-1Al2(SO4)3溶液中的离子总数为NA | |
| D. | 标准状况下,22.4mLH2O约含有 3.73NA个原子 |
13.亚硫酸及其盐在工业上具有广泛的用途.下面来解释亚硫酸及其盐的有关性质的方程式正确的是( )
0 160969 160977 160983 160987 160993 160995 160999 161005 161007 161013 161019 161023 161025 161029 161035 161037 161043 161047 161049 161053 161055 161059 161061 161063 161064 161065 161067 161068 161069 161071 161073 161077 161079 161083 161085 161089 161095 161097 161103 161107 161109 161113 161119 161125 161127 161133 161137 161139 161145 161149 161155 161163 203614
| A. | 亚硫酸水溶液的pH<7:H2SO3?2H++SO32- | |
| B. | 将亚硫酸滴入饱和Na2CO3溶液有气泡产生:2H++CO32-═H2O+CO2↑ | |
| C. | Na2SO3溶液能使红色石蕊变蓝:SO32-+H2O═HSO3-+OH- | |
| D. | Na2SO3溶液中加入足量的酸化Ba(NO3)2溶液出现白色沉淀:3SO32-+2NO3-+2H++3Ba2+═3BaSO4↓+2NO↑+H2O |