7.化学方程式可简明地体现元素及其化合物的性质.已知氧化还原反应:
2FeCl2+Cl2=2FeCl3
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
2FeCl3+2HI=2FeCl2+I2+2HCl;
复分解反应:2CH3COOH+K2CO3=2CH3COOK+CO2↑+H2O;
KCN+CO2+H2O=HCN+KHCO3
热分解反应:4KClO $\frac{\underline{\;\;△\;\;}}{\;}$3KCl+KClO4; KClO4 $\frac{\underline{\;\;△\;\;}}{\;}$KCl+2O2↑
根据以上反应分析下列说法正确是( )
2FeCl2+Cl2=2FeCl3
2Co(OH)3+6HCl=2CoCl2+Cl2↑+6H2O
2FeCl3+2HI=2FeCl2+I2+2HCl;
复分解反应:2CH3COOH+K2CO3=2CH3COOK+CO2↑+H2O;
KCN+CO2+H2O=HCN+KHCO3
热分解反应:4KClO $\frac{\underline{\;\;△\;\;}}{\;}$3KCl+KClO4; KClO4 $\frac{\underline{\;\;△\;\;}}{\;}$KCl+2O2↑
根据以上反应分析下列说法正确是( )
| A. | 还原性(酸性溶液):HCl>CoCl2>HI | B. | 酸性(水溶液):CH3COOH>HCN>H2CO3 | ||
| C. | 热稳定性:KCl<KClO4<KClO | D. | 氧化性(酸性溶液):Co(OH)3>FeCl3>I2 |
5.只能表示一个化学反应的离子方程式是( )
| A. | Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O | |
| B. | CO32-+2H+=H2O+CO2↑ | |
| C. | 2Br-+Cl2=2Cl-+Br2 | |
| D. | SO2+Cl2+2H2O=4H++2Cl-+SO42- |
20.在密闭容器中的一定量的混合气体发生反应:平衡xA(g)+yB(g)?zC(g)平衡时测得C的浓度为1mol•L-1,保持温度不变,将容器的容积扩大到原来的1倍,再达到平衡时,测得C的浓度为0.6mol•L-1,下列有关判断正确的是( )
| A. | x+y>z | B. | 平衡向逆反应方向移动 | ||
| C. | B的转化率降低 | D. | A的体积分数减小 |
19.铋(Bi)位于元素周期表中ⅤA族,+3价较稳定,铋酸钾(KBiO3)溶液呈无色.取一定量的硫酸锰(MnSO4)溶液依次滴加下列溶液,对应的现象如表所示:
关于KBiO3、KMnO4、I2、H2O2的氧化性由弱到强(从左至右)的顺序为( )
| 加入溶液 | ①适量的铋酸钾溶液 | ②过量的双氧水 | ③适量KI-淀粉溶液实验 |
| 现象 | 溶液呈紫红色 | 紫红色消失,产生气泡 | 溶液变成蓝色 |
| A. | KBiO3、KMnO4、H2O2、I2 | B. | KMnO4、KBiO3、I2、H2O2 | ||
| C. | I2、H2O2、KMnO4、KBiO3 | D. | H2O2、I2、KBiO3、KMnO4 |
18.下列说法没有科学性错误的是( )
0 160913 160921 160927 160931 160937 160939 160943 160949 160951 160957 160963 160967 160969 160973 160979 160981 160987 160991 160993 160997 160999 161003 161005 161007 161008 161009 161011 161012 161013 161015 161017 161021 161023 161027 161029 161033 161039 161041 161047 161051 161053 161057 161063 161069 161071 161077 161081 161083 161089 161093 161099 161107 203614
| A. | “白雪牌”漂白粉可令所有有色物质黯然失“色”,没有最白,只有更白 | |
| B. | CO有毒,生有煤炉的居室,可放置数盆清水,这样可有效地吸收CO,防止煤气中毒 | |
| C. | 氯化钙具有吸水性和潮解性,夏日里用它的水溶液喷洒柏油路,可有效地保护路面 | |
| D. | 氯元素有毒,禁止放入口中 |
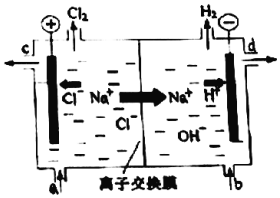 新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源,进行惰性电极电解饱和氯化钠溶液实验.回答下列问题:
新型高效的甲烷燃料电池采用铂为电极材料,两电极上分别通入CH4和O2,电解质为KOH溶液.某研究小组将甲烷燃料电池作为电源,进行惰性电极电解饱和氯化钠溶液实验.回答下列问题: