11.已知:①A+B2+═A2++B ②D+2H2O═D(OH)2+H2↑ ③以B、E为电极与E的盐溶液组成原电池,电极反应为:E2++2e-=E,B-2e-═B2+,下列说法正确的是( )
| A. | 氧化性:E2+>B2+>A2+>D2+ | |
| B. | 氧化性:D2+>E2+>A2+>B2+ | |
| C. | 反应E+A2+=A+E2+能够进行 | |
| D. | 提取某废水中含有少量的A2+时可以选用D |
10.碱性电池具有容量大,放电电流大的特点,因而得到广泛的应用.锌锰碱性电池以氢氧化钾溶液为电解液,电池总反应为:Zn+2MnO2+2H2O═Zn(OH)2+MnOOH,下列说法不正确的是( )
| A. | 电池工作时锌为负极 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电解液的OH-移向正极 | |
| D. | 外电路中每通过0.2mol电子,锌的质量理论上减少6.5g |
9.我国高速铁路技术世界领先.高速铁路的无缝钢轨是将钢轨间的接头用铝与氧化铁发生铝热反应进行焊接而成的.对于铝热反应:Fe2O3+2Al$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3,下列说法中正确的是( )
| A. | Fe元素的化合价升高 | B. | Al化合价升高 | ||
| C. | 该反应是化合反应 | D. | Al化合价没变 |
8.用下列实验方案及所选玻璃仪器(非玻璃仪器任选)就能实现相应实验目的是( )
| 实验目的 | 实验方案 | 所选玻璃仪器 | |
| A | 除去KNO3中少量NaCl | 将混合物制成热的饱和溶液,冷却结晶,过滤 | 酒精灯、烧杯、玻 璃棒 |
| B | 证明CH3COOH和HClO的酸性强弱 | 同温下用pH试纸测定浓度为0.1mol•L-1NaClO溶液和0.1mo•L-1 CH3COONa溶液的pH | 玻璃棒、玻璃片 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,再向其中加入新制的银氨溶液,并水浴加热 | 试管、烧杯、酒精 灯、滴管 |
| D | 配制1L 0.1mol•L-1 的CuSO4溶液 | 将25g CuSO4•5H2O溶解在一定量水中,配成1 L溶液 | 烧杯、量筒、玻璃 棒、容量瓶 (1000mL) |
| A. | A | B. | B | C. | C | D. | D |
7.已知25℃时,Ksp(BaSO4)=1.1×10-10.则在5.0%的Na2SO4溶液中(假设溶液的密度为1g•cm-3),Ba2+的最大浓度是( )
| A. | 4.2×10-10 mol•L-1 | B. | 8.4×10-10 mol•L-1 | ||
| C. | 3.1×10-10 mol•L-1 | D. | 5.8×10-10 mol•L-1 |
6.某溶液中含有Na+、Mg2+、Cl-、SO42-四种离子,已知Na+为0.2mol,Mg2+为0.4mol,Cl-为0.4mol,则SO42-物质的量为( )
| A. | 5mol | B. | 0.3mol | C. | 0.5mol | D. | 0.2mol |
3.下列化学式与指定物质的俗名对应正确的是( )
0 160882 160890 160896 160900 160906 160908 160912 160918 160920 160926 160932 160936 160938 160942 160948 160950 160956 160960 160962 160966 160968 160972 160974 160976 160977 160978 160980 160981 160982 160984 160986 160990 160992 160996 160998 161002 161008 161010 161016 161020 161022 161026 161032 161038 161040 161046 161050 161052 161058 161062 161068 161076 203614
| A. | CH3COOH--酒精 | B. | CO--水煤气 | C. | CaSO3--大理石 | D. | Na2CO3--纯碱 |
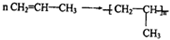
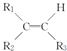 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$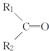 +R3-COOH,
+R3-COOH,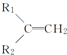 $\stackrel{KMnO_{4}(H+)}{→}$
$\stackrel{KMnO_{4}(H+)}{→}$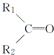 +CO2
+CO2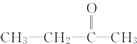 ),则此烯烃的结构简式是CH2=C(CH3)C2H5.
),则此烯烃的结构简式是CH2=C(CH3)C2H5.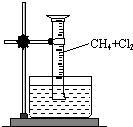 某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.
某研究小组为了探究甲烷和氯气反应的情况,设计了几个实验.