6.下列说法不正确的是( )
| A. | 干冰中分子的堆积方式为非密堆积 | |
| B. | 金属晶体中原子的最大配位数为12 | |
| C. | 晶体硅熔化时需破坏非极性共价键 | |
| D. | 冰融化为水的过程中其密度先变大,超过4℃后又逐渐变小 |
4.用NA表示阿佛加德罗常数的数值,下列判断正确的是( )
| A. | 标准状况下,8.0gSO3体积为2.24L | |
| B. | 物质的量为1molSO2、CO2的混合物所含氧原子数为2NA | |
| C. | 0.1molFeCl3溶液中含有的Fe3+数为0.1NA | |
| D. | 0.5mol镁在空气中完全燃烧所需要的氧气的物质的量为0.25mol |
3.设NA为阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 16gO2和O3的混合物中O原子的电子数为8NA | |
| B. | 标准状况下,2.24L氯气与水反应,转移的电子数为0.1NA | |
| C. | 28g乙烯与丙烯混合物中含有C-H键的数目为4NA | |
| D. | 常温下,1LpH=11的Na2CO3溶液中由水电离出H+的数目为0.001NA |
2.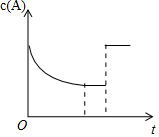 一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g)?xC(g)+3D(?),反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如图所示.下列有关说法正确的是( )
一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g)?xC(g)+3D(?),反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如图所示.下列有关说法正确的是( )
 一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g)?xC(g)+3D(?),反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如图所示.下列有关说法正确的是( )
一定温度下,将一定量的A、B气体充入密闭容器,发生反应:A(g)+B(g)?xC(g)+3D(?),反应平衡后,改变影响平衡的一个条件,物质A的浓度变化如图所示.下列有关说法正确的是( )| A. | x=2,C为气态,D可能为气态也可能为非气态 | |
| B. | 改变的条件可能是使用了催化剂 | |
| C. | 其他条件不变,若向容器中再加入少量C,平衡逆向移动但平衡常数不变 | |
| D. | 该反应的化学平衡常数K=$\frac{{c}^{2}(C)}{[c(A)•c(B)]}$,且温度升高,K值增大 |
20.下列叙述正确的是( )
| A. | 呈酸性的雨水通常称为酸雨 | |
| B. | 翡翠、玛瑙、水晶等饰物都是硅酸盐制品 | |
| C. | 合金材料一定全部由金属元素组成 | |
| D. | 硅是制作太阳能电池的主要原料 |
19.下列各组物质在适宜的条件下反应,其中氧化剂与还原剂物质的量之比为1:2的是( )
| A. | H2SO4(浓)+C | B. | Fe3O4+Al | C. | Cl2+Mg | D. | NO2+H2O |
18.下列实验事实不能用平衡移动原理解释的是( )
| A. |  将NO2球浸泡在冷水中和热水中 | |||||||||||||
| B. |  排饱和食盐水收集氯气 | |||||||||||||
| C. | 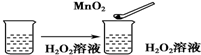 | |||||||||||||
| D. |
| |||||||||||||
17.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
0 160821 160829 160835 160839 160845 160847 160851 160857 160859 160865 160871 160875 160877 160881 160887 160889 160895 160899 160901 160905 160907 160911 160913 160915 160916 160917 160919 160920 160921 160923 160925 160929 160931 160935 160937 160941 160947 160949 160955 160959 160961 160965 160971 160977 160979 160985 160989 160991 160997 161001 161007 161015 203614
| A. | 1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.2NA | |
| B. | 在反应KClO3+6HCl=KCl+3Cl2+3H2O中,每生成3molCl2转移的电子数为6NA | |
| C. | 含4molSi-O键的二氧化硅晶体中,氧原子数为2NA | |
| D. | 某密闭容器中盛有0.2molSO2和0.1molO2,在一定条件下充分反应,生成SO2的分子数为0.2NA |
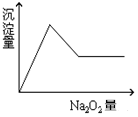 某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.