16.下列反应中,SO2做还原剂的是( )
| A. | 2Mg+SO2$\frac{\underline{\;△\;}}{\;}$2MgO+S | |
| B. | SO2+Br2+2H2O═2HBr+H2SO4 | |
| C. | Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O | |
| D. | SO2+2NaOH═Na2SO3+H2O |
15.下列仪器名称为“蒸馏烧瓶”的是( )
| A. |  | B. |  | C. |  | D. | 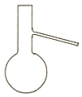 |
14.下列属于碱性氧化物的是( )
| A. | Ca(OH)2 | B. | Na2O | C. | SiO2 | D. | H2SO4 |
11.蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成.现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量.下列叙述正确的是( )
| A. | 沉淀X的成分是SiO2 | |
| B. | 将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3 | |
| C. | 在溶液Y中加入过量的NaOH溶液,过滤得到沉淀是Fe(OH)3 | |
| D. | 溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+ |
10.把一定量的铁铝合金平均分为两份,分别与足量硫酸和氢氧化钠溶液反应,结果放出H2的物质的量之比是3:1,则合金中铁与铝的物质的量之比为( )
| A. | 3:1 | B. | 1:3 | C. | 3:2 | D. | 2:3 |
9.下列鉴别物质或离子的方法能达到目的是( )
| A. | 用氨水鉴别MgCl2溶液和AlCl3溶液 | |
| B. | 用澄清石灰水鉴别Na2CO3溶液和NaHCO3溶液 | |
| C. | 用AgNO3鉴别Na2CO3溶液和NaCl溶液 | |
| D. | 用足量的盐酸和BaCl2溶液鉴别溶液中是否含SO42- |
8.工业上曾经通过反应“3Fe+4NaOH=Fe3O4+2H2↑+4Na↑”生产金属钠.下列有关说法正确的是( )
| A. | 不能用磁铁将Fe与Fe3O4分离 | |
| B. | 将生成的气体在空气中冷却可获得钠 | |
| C. | 该反应条件下铁的氧化性比钠强 | |
| D. | 该反应中每生成2 mol H2,转移的电子数约为4×6.02×1023 |
7.下列离子方程式正确的是( )
0 160779 160787 160793 160797 160803 160805 160809 160815 160817 160823 160829 160833 160835 160839 160845 160847 160853 160857 160859 160863 160865 160869 160871 160873 160874 160875 160877 160878 160879 160881 160883 160887 160889 160893 160895 160899 160905 160907 160913 160917 160919 160923 160929 160935 160937 160943 160947 160949 160955 160959 160965 160973 203614
| A. | 氢氧化钡中加入稀硫酸:Ba2++OH-+SO42-+H+═BaSO4↓+H2O | |
| B. | 将大理石投入到足量盐酸中:CO32-+2H+═CO2↑+H2O | |
| C. | 次氯酸钙溶液中通入少量二氧化碳:Ca2++2ClO-+H2O+CO2═CaCO3↓+2HClO | |
| D. | 硫酸镁溶液和氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ |
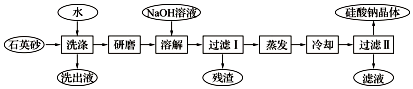
 .
.