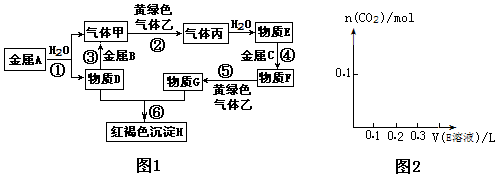
18.“变化观念与平衡思想”是化学学科的核心素养,室温时0.10mol/L草酸钠溶液中存在多个平衡,其中有关说法正确的是【已知室温时,Ksp(CaC2O4)=2.4×10-9】( )
| A. | 若将溶液不断加水稀释,则水的电离程度增大 | |
| B. | 溶液中各离子浓度大小关系c(Na+)>c(C2O42-)>c(OH-)>c(H+)>c(HC2O4-) | |
| C. | 若用pH计测得溶液的pH=a,则H2C2O4的第二级电离平衡常数Ka2=1013-2a | |
| D. | 向溶液中加入等体积CaCl2溶液,当加入的CaCl2溶液浓度大于2.4×10-8mol/L时即能产生沉淀 |
17.下列有关有机化合物结构和性质的说法正确的是( )
| A. | 乙烯、苯和乙酸均能发生加成反应 | |
| B. | 某芳香烃的分子式为C10H14,它可使酸性 KMnO4溶液褪色,且分子结构中只有一个侧链,符合条件的烃有4种 | |
| C. | 1 mol的有机物(结构如图)最多能与含5mol NaOH的水溶液完全反应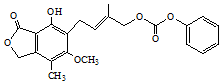 | |
| D. | 油脂皂化反应得到高级脂肪酸与甘油 |
16.短周期元素甲、乙、丙、丁的原子序数依次增大,甲的L层电子数是K层的3倍,丁所在族序数是周期数的2倍,乙、丙、丁的最外层电子数之和为10.下列说法正确的是( )
| A. | 简单离子半径:乙>丙>丁>甲 | |
| B. | 简单气态氢化物的稳定性:甲>丁,这是因为甲的氢化物分子间存在氢键 | |
| C. | 甲和丁组成的化合物在熔融状态下可以导电 | |
| D. | 乙、丙、丁的最高价氧化物对应的水化物均能两两反应 |
15.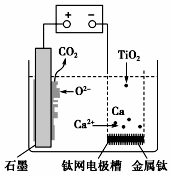 研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中错误的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中错误的是( )
 研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中错误的是( )
研究发现,可以用石墨作阳极、钛网作阴极、熔融的CaF2-CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化钛制备金属钛.下列说法中错误的是( )| A. | 在制备金属钛前后,整套装置中CaO的总量保持不变 | |
| B. | 阳极的电极反应式为C+2O2--4e-═CO2↑ | |
| C. | 由TiO2制得1 mol金属Ti,理论上外电路通过2 mol 电子 | |
| D. | 若用铅蓄电池作供电电源,“-”接线柱应连接Pb电极 |
14.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 64gCaC2中含有的共价键数目为3NA | |
| B. | 20gD2O与20gH218O含有的中子数均为11NA | |
| C. | 4.6gNO2在标准状况下,含有的分子数为0.1 NA | |
| D. | 50ml 12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA |
13.化学与科学、技术、社会、环境密切相关.下列叙述不正确的是( )
| A. | 大气中PM2.5比表面积大,吸附力强,能吸附许多有毒、有害物质 | |
| B. | 氯气分别和氢氧化钠溶液、石灰乳反应得到的所有含氯化合物都具有漂白性 | |
| C. | 石墨烯是一种由单层碳原子构成的新纳米材料,具有导电性 | |
| D. | 刚玉、红宝石主要成分是氧化铝,陶瓷、分子筛主要成分是硅酸盐 |
10.同温同压下,等质量的甲烷(CH4)和N2O两种气体相比较,下列叙述中正确的( )
| A. | 物质的量之比为1:1 | B. | 密度之比为4:11 | ||
| C. | 体积之比为4:11 | D. | 原子数之比为5:3 |
9.下列离子方程式书写正确的是( )
0 160704 160712 160718 160722 160728 160730 160734 160740 160742 160748 160754 160758 160760 160764 160770 160772 160778 160782 160784 160788 160790 160794 160796 160798 160799 160800 160802 160803 160804 160806 160808 160812 160814 160818 160820 160824 160830 160832 160838 160842 160844 160848 160854 160860 160862 160868 160872 160874 160880 160884 160890 160898 203614
| A. | AlCl3溶液与过量的氨水反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| B. | 过量的澄清石灰水与碳酸氢钠溶液反应:2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O | |
| C. | 硫酸与Ba(OH)2溶液反应:H++OH-=H2O | |
| D. | FeCl3溶液与Fe反应:Fe3++Fe=2Fe2+ |