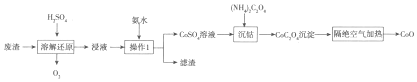
4.有关氯化钠叙述错误的是( )
| A. | 是强电解质 | B. | 固体能导电 | ||
| C. | 电子式为: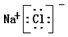 | D. | 25℃时,溶液的pH=7 |
3.一定含有离子的物质是( )
| A. | I2 | B. | CH3CH2OH | C. | HCl | D. | KCl |
1. 向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
 向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )| A. | 原溶液中MgCl2和CuCl2的物质的量浓度相等 | |
| B. | 该实验不能证明Cu(OH)2的Ksp比Mg(OH)2的Ksp小 | |
| C. | 水的电离程度:A>B>C | |
| D. | 若向Mg(OH)2悬浊液中加入CuCl2溶液,一定会有Cu(OH)2生成 |
20.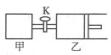 如图所示,关闭活塞,向甲、乙两刚性密闭容器中分别充入1mol A、2mol B,此时甲、乙的容积均为2L(连通管体积忽略不计).在T℃时,两容器中均发生下述反应:A(g)+2B(g)?2C(g)+3D(g),△H<0.达平衡时,乙的体积为2.6L,下列说法正确的是( )
如图所示,关闭活塞,向甲、乙两刚性密闭容器中分别充入1mol A、2mol B,此时甲、乙的容积均为2L(连通管体积忽略不计).在T℃时,两容器中均发生下述反应:A(g)+2B(g)?2C(g)+3D(g),△H<0.达平衡时,乙的体积为2.6L,下列说法正确的是( )
 如图所示,关闭活塞,向甲、乙两刚性密闭容器中分别充入1mol A、2mol B,此时甲、乙的容积均为2L(连通管体积忽略不计).在T℃时,两容器中均发生下述反应:A(g)+2B(g)?2C(g)+3D(g),△H<0.达平衡时,乙的体积为2.6L,下列说法正确的是( )
如图所示,关闭活塞,向甲、乙两刚性密闭容器中分别充入1mol A、2mol B,此时甲、乙的容积均为2L(连通管体积忽略不计).在T℃时,两容器中均发生下述反应:A(g)+2B(g)?2C(g)+3D(g),△H<0.达平衡时,乙的体积为2.6L,下列说法正确的是( )| A. | 甲中反应的平衡常数小于乙 | |
| B. | 当乙中A与B的体积分数之比为1:2时,反应达到平衡状态 | |
| C. | 平衡时甲容器中A的物质的量小于0.55 mol | |
| D. | 若打开活塞K,达平衡时乙容器的体积为3.2 L |
19.次磷酸(H3PO2)是一种具有强还原性的一元弱酸,工业上常利用H3PO2和AgNO3溶液反应进行化学镀银,已知该反应中氧化剂与还原剂的物质的量之比为4:1,则下列说法中不正确的是( )
| A. | H3PO2中磷元素的化合价为+1 | |
| B. | H3PO2的电离方程式为H3PO2?H++H2 PO2- | |
| C. | H3PO2被AgNO3氧化成了H3PO4 | |
| D. | NaH2PO2、NaH2PO4、Na2HPO4均为酸式盐 |
18.下列反应既是氧化还原反应,又是吸热反应的是( )
| A. | 铝粉与WO3共热制备金属钨 | B. | 高温下CO还原Fe2O3制备铁 | ||
| C. | 铁粉与水蒸气加热制备氢气 | D. | Ca( OH)2与NH4Cl加热制备氨气 |
17.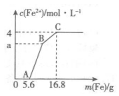 某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )
某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )
 某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )
某100mL稀溶液中只含有Fe3+、Cu2+、H+、NO3-四种离子,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的质量的关系如图所示,若整个反应过程中溶液的体积不发生变化,则下列说法中不正确的是( )| A. | 原溶液的c(H+)=4 mol•L-1 | |
| B. | 若a=3,则原溶液中c(Cu2+)=1 mol•L-1 | |
| C. | 原溶液中的c(NO3)=7 mol•L-1 | |
| D. | BC段发生反应的离子方程式为Cu2++Fe═Fe2++Cu |
16.下列储存药品的方法中,正确的是( )
| A. | 液溴保存在带橡胶塞的玻璃瓶中 | |
| B. | 新制氯水保存在棕色广口瓶中 | |
| C. | 金属锂保存在石蜡油中 | |
| D. | 硅酸钠溶液保存在带磨口玻璃塞的玻璃瓶中 |
15.W、X、Y、Z是原子序数依次增大的短周期元素,W是原子半径最小的短周期元素,W、Y同主族,X、Z同主族,且X、Z的原子序数之和是W、Y原子序数之和的2倍.下列说法中不正确的是( )
0 160691 160699 160705 160709 160715 160717 160721 160727 160729 160735 160741 160745 160747 160751 160757 160759 160765 160769 160771 160775 160777 160781 160783 160785 160786 160787 160789 160790 160791 160793 160795 160799 160801 160805 160807 160811 160817 160819 160825 160829 160831 160835 160841 160847 160849 160855 160859 160861 160867 160871 160877 160885 203614
| A. | W和X形成的化合物可能含有非极性共价键 | |
| B. | X和Z形成的化合物常温下为固态 | |
| C. | W、X、Y、Z四种元素组成的化合物的水溶液可能呈酸性 | |
| D. | W、X、Y、Z四种元素两两之间均能形成二元化合物 |