15.下列离子方程式书写正确的是( )
| A. | 往碳酸钙溶液中滴加稀盐酸:CO32-+2H+═CO2↑+H2O | |
| B. | 向次氯酸钙溶液通入少量SO2:Ca2++3ClO-+SO2+H2O═CaSO4↓+Cl-+2HClO | |
| C. | 少量金属钠加到冷水中:Na+2H2O═Na++OH-+H2↑ | |
| D. | 向NH4HCO3溶液中加过量的NaOH溶液并加热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O |
14.下列说法中,正确的是( )
| A. | 甲醛、乙醛、丙醛都没有同分异构体 | |
| B. | 已知甲醛是平面型分子,则苯甲醛的所有原子有可能在同一平面上 | |
| C. | 甲醛、乙醛、苯甲醛都能发生加成、氧化和酯化反应 | |
| D. | 可用新制的Cu(OH)2来区分甲醛和苯甲醛 |
12.不能使橙色溴水变为无色的是( )
| A. | NaOH溶液 | B. | 用CCl4多次萃取 | C. | 锌粉 | D. | KI溶液 |
11.已知1gH2完全燃烧生成水蒸气放出热量为121kJ,有关数据如下:O=O(键能为496kJ•mol-1)、H-H(键能为436kJ•mol-1),试求H2O(g)中H-O键的键能为( )
| A. | 463kJ•mol-1 | B. | 926kJ•mol-1 | C. | 1852kJ•mol-1 | D. | 920kJ•mol-1 |
8.将Na2O2粉末投入下列物质的饱和溶液中,恢复到室温,最终不一定产生沉淀的是( )
| A. | FeCl2 | B. | AlCl3 | C. | MgCl2 | D. | NaCl |
6.以赤铁矿(主要成分为60.0%Fe2O3,杂质有3.6%FeO,Al2O3,MnO2,CuO等)为原料制备高活性铁单质的主要生产流程如图所示:
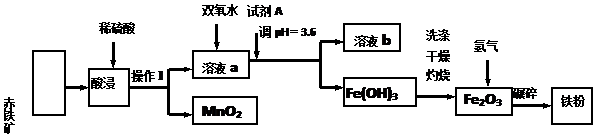
已知部分阳离子以氢氧化物形式完全深沉时溶液的pH如表所示,请回答下列问题:
(1)含杂质的赤铁矿使用前要将其粉碎,目的是增大固液接触面积,加快浸出反应速率,提高浸出率.操作Ⅰ的名称是过滤.
(2)将操作Ⅰ后所得的MnO2与KClO3、KOH溶液混合共热,可得到K2MnO4,此反应的化学方程式是3MnO2+KClO3+6KOH$\frac{\underline{\;\;△\;\;}}{\;}$3K2MnO4+KCl+3H2O.
(3)将PH控制在3.6的目的是使铁离子全部沉淀下来而其他金属离子不沉淀.已知25℃时,Ksp[Cu(OH)2]=2×10-20,该温度下反应Cu2++2H2O?Cu(OH)2+2H+的平衡常数K=5×10-9.
(4)加入双氧水时反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(5)利用氨气在500℃以上分解得到的氮原子渗透到铁粉中可制备氮化铁(FexVy),若消耗氨气17.0g,消耗赤铁矿石1Kg,写出该反应完整的化学方程式:16Fe+2NH3$\frac{\underline{\;大于500℃\;}}{\;}$2Fe8N+3H2.
0 160617 160625 160631 160635 160641 160643 160647 160653 160655 160661 160667 160671 160673 160677 160683 160685 160691 160695 160697 160701 160703 160707 160709 160711 160712 160713 160715 160716 160717 160719 160721 160725 160727 160731 160733 160737 160743 160745 160751 160755 160757 160761 160767 160773 160775 160781 160785 160787 160793 160797 160803 160811 203614

已知部分阳离子以氢氧化物形式完全深沉时溶液的pH如表所示,请回答下列问题:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe (OH)2 | Cu (OH)2 |
| pH | 3.4 | 5.2 | 9.7 | 6.7 |
(2)将操作Ⅰ后所得的MnO2与KClO3、KOH溶液混合共热,可得到K2MnO4,此反应的化学方程式是3MnO2+KClO3+6KOH$\frac{\underline{\;\;△\;\;}}{\;}$3K2MnO4+KCl+3H2O.
(3)将PH控制在3.6的目的是使铁离子全部沉淀下来而其他金属离子不沉淀.已知25℃时,Ksp[Cu(OH)2]=2×10-20,该温度下反应Cu2++2H2O?Cu(OH)2+2H+的平衡常数K=5×10-9.
(4)加入双氧水时反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O.
(5)利用氨气在500℃以上分解得到的氮原子渗透到铁粉中可制备氮化铁(FexVy),若消耗氨气17.0g,消耗赤铁矿石1Kg,写出该反应完整的化学方程式:16Fe+2NH3$\frac{\underline{\;大于500℃\;}}{\;}$2Fe8N+3H2.
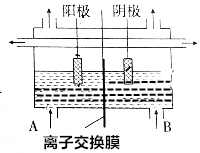 工业上电解饱和食盐水的方法之一是将两个电极室用离子交换膜隔开(如图所示),其目的是防止H2与Cl2混合发生爆炸,防止Cl2与NaOH反应生成NaClO,使NaOH不纯,阳极室(A处)加入饱和食盐水,阴极室(B极)加入水或稀氢氧化钠溶液,离子交换膜只许Na+离子通过.
工业上电解饱和食盐水的方法之一是将两个电极室用离子交换膜隔开(如图所示),其目的是防止H2与Cl2混合发生爆炸,防止Cl2与NaOH反应生成NaClO,使NaOH不纯,阳极室(A处)加入饱和食盐水,阴极室(B极)加入水或稀氢氧化钠溶液,离子交换膜只许Na+离子通过.
 某研究小组取一定质量的镁铝合金材料投入200mL稀硫酸中,待固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.请回答下列问题
某研究小组取一定质量的镁铝合金材料投入200mL稀硫酸中,待固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示.请回答下列问题