15. 溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:
溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:
①合成反应:在仪器B中加入适量NaBr、浓硫酸和50ml乙醇,安装好仪器,缓缓加热,收集馏出物.
②分离提纯:将馏出物加水后振荡,再加入适量酸除去乙醚,分液,最后得到52mL溴乙烷.
回答下列问题:
(1)仪器B的名称是蒸馏烧瓶,B中发生的主要反应有:NaBr+H2SO4=NaHSO4+HBr,以及HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O
(2)仪器C为直形冷凝管,冷水进口是b(填“a”或“b”)
(3)仪器D置于盛有冰水混合的烧杯中,目的是冷却溴乙烷
(4)溴乙烷粗产品分离提纯阶段,加水的目的是除去溶解在溴乙烷中乙醇
(5)该实验所得溴乙烷的产率为79%.
 溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:
溴乙烷是一种重要的化工合成原料.实验室合成溴乙烷的实验装置如下:实验中可能用到的数据如表:| 物 质 | 相对分子质量 | 沸点(℃) | 密度(g•cm-3) | 水溶性 |
| CH3CH2OH | 46 | 78.4 | 0.79 | 互溶 |
| CH3CH2Br | 109 | 38.4 | 1.42 | 难溶 |
| CH3CH2OCH2CH3 | 74 | 34.5 | 0.71 | 微溶 |
| CH2=CH2 | 28 | -103.7 | 0.38 | 不溶 |
| 浓硫酸(H2SO4) | 98 | 338.0 | 1.38 | 易溶 |
②分离提纯:将馏出物加水后振荡,再加入适量酸除去乙醚,分液,最后得到52mL溴乙烷.
回答下列问题:
(1)仪器B的名称是蒸馏烧瓶,B中发生的主要反应有:NaBr+H2SO4=NaHSO4+HBr,以及HBr+CH3CH2OH$\stackrel{△}{→}$CH3CH2Br+H2O
(2)仪器C为直形冷凝管,冷水进口是b(填“a”或“b”)
(3)仪器D置于盛有冰水混合的烧杯中,目的是冷却溴乙烷
(4)溴乙烷粗产品分离提纯阶段,加水的目的是除去溶解在溴乙烷中乙醇
(5)该实验所得溴乙烷的产率为79%.
13.下列实验能获得成功的是( )
| A. | 用溴水可鉴别苯、乙醇、苯乙烯 | |
| B. | 将乙烷和氯气的混合气放在光照条件下反应制备氯乙烷(C2H5Cl) | |
| C. | 苯、溴水、铁粉混合制成溴苯 | |
| D. | 检验氯代烃中含氯,加NaOH溶液加热后,用稀硫酸酸化,再检验 |
12.由乙醇及必要的无机试剂合成乙二醇,其依次发生的反应类型为( )
| A. | 取代,消去,加成 | B. | 加成,消去,取代 | C. | 消去,加成,取代 | D. | 取代,加成,消去 |
7.在密闭容器中发生下列反应aA(g)?cC(g)+dD(g),反应达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的2.1倍,下列叙述不正确的是( )
| A. | A的转化率变大 | B. | a<c+d | ||
| C. | A的质量分数变小 | D. | 平衡向正反应方向移动 |
6.已知石墨的燃烧热为△H1,金刚石的燃烧热为△H2,下列说法正确的是( )
0 160609 160617 160623 160627 160633 160635 160639 160645 160647 160653 160659 160663 160665 160669 160675 160677 160683 160687 160689 160693 160695 160699 160701 160703 160704 160705 160707 160708 160709 160711 160713 160717 160719 160723 160725 160729 160735 160737 160743 160747 160749 160753 160759 160765 160767 160773 160777 160779 160785 160789 160795 160803 203614
| A. | 由于石墨和金刚石属于不同的单质,所以△H1和△H2不等 | |
| B. | 由于燃烧反应放热,所以△H1和△H2均取正值 | |
| C. | 由于石墨和金刚石同为碳元素组成,所以△H1=△H2 | |
| D. | 由于燃烧均为放热反应,所以石墨为重要的能源 |
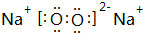 .
.
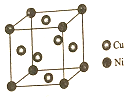 东晋《华阳国志南中志》卷四种已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题:
东晋《华阳国志南中志》卷四种已有关于白铜的记载,云南镍白铜(铜镍合金)文明中外,曾主要用于造币,亦可用于制作仿银饰品.回答下列问题: