6.下列各组中的离子能大量共存的是( )
| A. | Ba2+、Na+、NO3-、SO42- | B. | Mg2+、NH4+、NO3-、SO42- | ||
| C. | NH4+、K+、Cl-、OH- | D. | K+、H+、SO32-、ClO- |
5.如表周期表中的一部分,根据A~Ⅰ在周期表中的位置,用元素符号或化学式回答下列问题.
(1)化学性质员不活泼的元素是Ne,只有负价而无正价的元素是F,最容易与氢气反应的单质是F2,金属性最强的单质是Na.
(2)地壳中含量最多的元素是O,化合物种类最多的元素是C,与水反应最激烈的金属是Na,单质可以用于制漂白粉的元素是Cl2.
(3)在B、C、D、E、F、G、H中,原子半径最大的元素是Na
(4)A和E形成化合物的电子式是 .
.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)地壳中含量最多的元素是O,化合物种类最多的元素是C,与水反应最激烈的金属是Na,单质可以用于制漂白粉的元素是Cl2.
(3)在B、C、D、E、F、G、H中,原子半径最大的元素是Na
(4)A和E形成化合物的电子式是
 .
.
4.根据下列操作及现象,所得结论正确的是( )
| 选项 | 操作及现象 | 结论 |
| A | 将0.1mol•L-1氨水稀释成0.01mol•L-1,测得pH由11.1变成10.6 | 稀释后NH3•H2O的电离程度减小 |
| B | 将铜片与锌片用导线连接后,插入稀硫酸中,铜片上有气泡产生 | 在锌的作用下,铜与硫酸反应产生氢气 |
| C | 向25mL冷水和沸水中分别滴入5滴FeCl3饱和溶液,前者为黄色,后者为红褐色 | 温度升高,Fe3+的水解程度增大 |
| D | 将固体CaSO4加入Na2CO3饱和溶液中,一段时间后,检验固体成分为CaCO3 | 同温下溶解度:CaSO4<CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
3.关于下列各装置图的叙述中,不正确的是( )
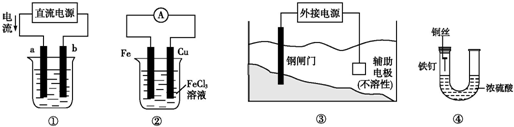

| A. | 用装置①精炼铜,则a极为精铜,电解质溶液为CuSO4溶液 | |
| B. | 装置②的总反应是:Fe+2Fe3+═3Fe2+ | |
| C. | 装置③中钢闸门应与外接电源的负极相连 | |
| D. | 装置④中的铁钉几乎没被腐蚀 |
18.80℃时,将0.40mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4(g)?2NO2(g)△H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
(1)计算20~40s 内用N2O4表示的平均反应速率为0.002 mol•L-1•s-1.
(2)计算在80℃时该反应的平衡常数K=1.8.
(3)反应进行至100s 后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”、“变深”或“不变”).
(4)要增大该反应的K值,可采取的措施有D(填序号).
A.增大N2O4 起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度.
0 160587 160595 160601 160605 160611 160613 160617 160623 160625 160631 160637 160641 160643 160647 160653 160655 160661 160665 160667 160671 160673 160677 160679 160681 160682 160683 160685 160686 160687 160689 160691 160695 160697 160701 160703 160707 160713 160715 160721 160725 160727 160731 160737 160743 160745 160751 160755 160757 160763 160767 160773 160781 203614
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
(2)计算在80℃时该反应的平衡常数K=1.8.
(3)反应进行至100s 后将反应混合物的温度降低,混合气体的颜色变浅(填“变浅”、“变深”或“不变”).
(4)要增大该反应的K值,可采取的措施有D(填序号).
A.增大N2O4 起始浓度
B.向混合气体中通入NO2
C.使用高效催化剂
D.升高温度.
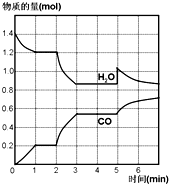 在一容积为2L的密闭容器中,高温下发生下列反应:C(s)+H2O(g)?CO(g)+H2(g),其中H2O、CO的物质的量(mol)随时间(min)的变化曲线如图所示:
在一容积为2L的密闭容器中,高温下发生下列反应:C(s)+H2O(g)?CO(g)+H2(g),其中H2O、CO的物质的量(mol)随时间(min)的变化曲线如图所示: