6.下表为元素周期表的一部分,请按要求回答问题:
(1)表中元素F的非金属性最强,元素Na的金属性最强(填元素符号).
(2)表中元素③的原子结构示意图 ;元素⑨形成的氢化物的电子式
;元素⑨形成的氢化物的电子式 .
.
(3)表中元素④、⑨形成的氢化物的稳定性顺序为HF>HCl(填化学式).
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为HClO4>H2SO4(填化学式).
(5)表中元素③、④、⑥、⑦的原子半径大小为Na>Mg>O>F(填元素符号).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)表中元素③的原子结构示意图
 ;元素⑨形成的氢化物的电子式
;元素⑨形成的氢化物的电子式 .
.(3)表中元素④、⑨形成的氢化物的稳定性顺序为HF>HCl(填化学式).
(4)表中元素⑧和⑨的最高价氧化物对应水化物的酸性强弱为HClO4>H2SO4(填化学式).
(5)表中元素③、④、⑥、⑦的原子半径大小为Na>Mg>O>F(填元素符号).
4.在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)═zC(g),图I表示200℃时容器中A、B、C物质的量随时间的变化,图Ⅱ表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )
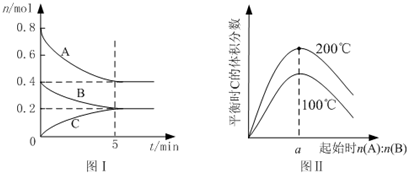

| A. | 200℃时,反应从开始到平衡的平均速率v(B)=0.04mol•L-1•min-1 | |
| B. | 图Ⅱ所知反应xA(g)+yB(g)?zC(g)+Q(Q>0) | |
| C. | 若在图Ⅰ所示的平衡状态下,再向体系中充入He,重新达到平衡前v(正)>v(逆) | |
| D. | 由图I可知,该反应式为2A(g)+B(g)?C(g) |
2. 碳及其化合物应用广泛.
碳及其化合物应用广泛.
I.工业上利用CO和水蒸汽反应制氢气,存在以下平衡:
CO(g)+H2O(g)$\stackrel{沸石分子筛}{?}$CO2(g)+H2(g)
(1)沸石分子筛中含有硅元素,请写出硅原子结构示意图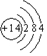 (2)向1L恒容密闭容器中注人CO和H2O(g),830℃时测得部分数据如表.
(2)向1L恒容密闭容器中注人CO和H2O(g),830℃时测得部分数据如表.
则该温度下反应的平衡常数K=1
(3)相同条件下,向1L恒容密闭容器中,同时注人1m o l CO、1mol H2O (g),2molCO2和2mo1H2,此时v(正 )< v(逆)(填“>”“=”或“<”)
II.已知CO(g)+$\frac{1}{2}$O2 (g)= CO2 (g)△H=-141kJ•mol-1
2H2 (g)+O2(g)= 2H2o (g)△H=-484kJ•mol-1
CH3OH(1)+$\frac{3}{2}$O2(g)=CO2 (g)+2H2O (g)△H=-726kJ•mol-1'
(4)利用CO、H2化合制得液态甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(l)△H=+101kJ/mol
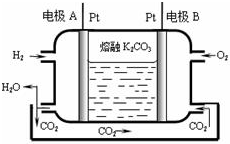
III.一种新型氢氧燃料电池工作原理如图所示
(5)写出电极A的电极反应式H2-2e-+CO32-=CO2+H2O
(6)以上述电池电解饱和食盐水,若生成0.2mo1 Cl2,则至少需通入O2的体积为2.24L(标准状况)
 碳及其化合物应用广泛.
碳及其化合物应用广泛.I.工业上利用CO和水蒸汽反应制氢气,存在以下平衡:
CO(g)+H2O(g)$\stackrel{沸石分子筛}{?}$CO2(g)+H2(g)
(1)沸石分子筛中含有硅元素,请写出硅原子结构示意图
 (2)向1L恒容密闭容器中注人CO和H2O(g),830℃时测得部分数据如表.
(2)向1L恒容密闭容器中注人CO和H2O(g),830℃时测得部分数据如表.| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| n(CO)/mol | 0.200 | 0.160 | 0.125 | 0.099 | 0.080 | 0.080 |
| n(H2O)/mol | 0.300 | 0.260 | 0.225 | 0.199 | 0.180 | 0.180 |
(3)相同条件下,向1L恒容密闭容器中,同时注人1m o l CO、1mol H2O (g),2molCO2和2mo1H2,此时v(正 )< v(逆)(填“>”“=”或“<”)
II.已知CO(g)+$\frac{1}{2}$O2 (g)= CO2 (g)△H=-141kJ•mol-1
2H2 (g)+O2(g)= 2H2o (g)△H=-484kJ•mol-1
CH3OH(1)+$\frac{3}{2}$O2(g)=CO2 (g)+2H2O (g)△H=-726kJ•mol-1'
(4)利用CO、H2化合制得液态甲醇的热化学方程式为CO(g)+2H2(g)=CH3OH(l)△H=+101kJ/mol
III.一种新型氢氧燃料电池工作原理如图所示
(5)写出电极A的电极反应式H2-2e-+CO32-=CO2+H2O
(6)以上述电池电解饱和食盐水,若生成0.2mo1 Cl2,则至少需通入O2的体积为2.24L(标准状况)
1.氮的氢化物NH3、N2H4等在工农业生产、航空航天等领域有广泛应用.
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2 (g)=4NO (g)+6H2O (L)△H1
②4NH3(g)+6NO(g)=5N2 (g)+6H2O (L)△H2
则反应 4NH3(g)+3O2(g)=2N2 (g)+6H2O (L)△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol N2 在一定条件下合成氮,平衡时仅改变温度测得的数据如下表所示:
已知:破坏1mol N2(g)和3mol H2(g)中的化学键消耗的总能量小于破坏2mol NH3(g)中的化学键消耗的能量.
①则 T1、<T2(填“>”、“<”或“=”)
②T2K下,经过10min达到化学平衡状态,则o~10min内H2的平均速率v(H2)=0.1mol•L-1•min-1.
③下列图象分别代表焓变(△H),混合气体平均相对分子质量($\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态是BC.

(3)电化学降解治理水中硝酸盐污染,在酸性条件下,电化学降解NO3-的原理如图1,阴极反应式为2NO3-+12H++10e-=N2↑+6H2O.

(4)通过控制溶液的pH对工业废水中的金属离子进行分离.图2是某些金属氢氧化物在不同浓度和pH的沉淀--溶解图象,图中直线上的点表示平衡状态.当溶液中的离子浓度小于1×10-5mol•L-1时,认为该离子沉淀完全.
由图可知Cu(OH)2的浓度积的值为1×10-21.8.
0 160565 160573 160579 160583 160589 160591 160595 160601 160603 160609 160615 160619 160621 160625 160631 160633 160639 160643 160645 160649 160651 160655 160657 160659 160660 160661 160663 160664 160665 160667 160669 160673 160675 160679 160681 160685 160691 160693 160699 160703 160705 160709 160715 160721 160723 160729 160733 160735 160741 160745 160751 160759 203614
(1)液氨作为一种潜在的清洁汽车燃料已越来越被研究人员重视.它在安全性、价格等方较化石燃料和氢燃料有着较大的优势.氨的燃烧实验涉及下列两个相关的反应:
①4NH3(g)+5O2 (g)=4NO (g)+6H2O (L)△H1
②4NH3(g)+6NO(g)=5N2 (g)+6H2O (L)△H2
则反应 4NH3(g)+3O2(g)=2N2 (g)+6H2O (L)△H=$\frac{3△{H}_{1}+2△{H}_{2}}{5}$(请用含有△H1、△H2的式子表示)
(2)合成氨实验中,在体积为3L的恒容密闭容器中,投入4mol N2和9mol N2 在一定条件下合成氮,平衡时仅改变温度测得的数据如下表所示:
| 温度(K) | 平衡时NH3的物质的量(mol) |
| T1 | 2.4 |
| T2 | 2.0 |
①则 T1、<T2(填“>”、“<”或“=”)
②T2K下,经过10min达到化学平衡状态,则o~10min内H2的平均速率v(H2)=0.1mol•L-1•min-1.
③下列图象分别代表焓变(△H),混合气体平均相对分子质量($\overline{M}$)、N2体积分数φ(N2)和气体密度(ρ)与反应时间的关系,其中正确且能表明该可逆反应达到平衡状态是BC.

(3)电化学降解治理水中硝酸盐污染,在酸性条件下,电化学降解NO3-的原理如图1,阴极反应式为2NO3-+12H++10e-=N2↑+6H2O.

(4)通过控制溶液的pH对工业废水中的金属离子进行分离.图2是某些金属氢氧化物在不同浓度和pH的沉淀--溶解图象,图中直线上的点表示平衡状态.当溶液中的离子浓度小于1×10-5mol•L-1时,认为该离子沉淀完全.
由图可知Cu(OH)2的浓度积的值为1×10-21.8.

 合理应用和处理氮的化合物,在生产生活中有重要意义.
合理应用和处理氮的化合物,在生产生活中有重要意义.