5.运用化学反应原理研究碳、氮、硫等单质及其化合物的反应有重要的意义.
(1)CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)═CH3CH2OH(g)+3H2O(g)△H=QkJ/mol (Q>0)
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如图1所示.
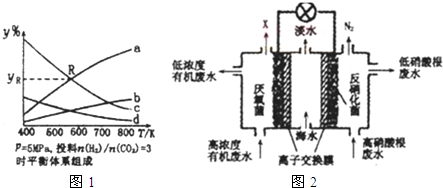
完成下列填空:
①图中曲线a表示的是H2O的体积分数.
②图中曲线a和c的交点R对应物质的体积分数yR=37.5%.
(2)25° C,H2SO3和H2CO3两种酸的电离平衡常数如表.
将足量的NaHSO溶液加人到Na2CO3溶液中,反应的离子方程式为CO32-+HSO3-=HCO3-+SO32-
(3)工业上用可溶性碳酸盐提取锶时,先将SrSO4转化为难溶弱酸盐,再处理.
SrSO4?Sr2+(aq)+SO${\;}_{4}^{2-}$(aq) Ksp=2.5×10-7
SrCO3?Sr2+(aq)+CO${\;}_{3}^{2-}$(aq) Ksp=2.5×10-9
则SrSO4转化为SrCO3反应的平衡常数值为100
(4)图2是一种三室微生物燃料电池污水净化系统原理示意图,同时处理有机废水和硝酸盐废水,并获得淡水,图中有机废水中有机物可用C6H10O5表示.
①产生N2的电极为电池的正极(填“正”或“负”).
②生成X(气体)的电极上发生的电极反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+.
(1)CO2为碳源制取低碳有机物成为国际研究焦点,下面为CO2加氢制取乙醇的反应:
2CO2(g)+6H2(g)═CH3CH2OH(g)+3H2O(g)△H=QkJ/mol (Q>0)
在密闭容器中,按CO2与H2的物质的量之比为1:3进行投料,在5MPa下测得不同温度下平衡体系中各种物质的体积分数(y%)如图1所示.

完成下列填空:
①图中曲线a表示的是H2O的体积分数.
②图中曲线a和c的交点R对应物质的体积分数yR=37.5%.
(2)25° C,H2SO3和H2CO3两种酸的电离平衡常数如表.
| K1 | K2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.4×10-7 | 4.7×10-11 |
(3)工业上用可溶性碳酸盐提取锶时,先将SrSO4转化为难溶弱酸盐,再处理.
SrSO4?Sr2+(aq)+SO${\;}_{4}^{2-}$(aq) Ksp=2.5×10-7
SrCO3?Sr2+(aq)+CO${\;}_{3}^{2-}$(aq) Ksp=2.5×10-9
则SrSO4转化为SrCO3反应的平衡常数值为100
(4)图2是一种三室微生物燃料电池污水净化系统原理示意图,同时处理有机废水和硝酸盐废水,并获得淡水,图中有机废水中有机物可用C6H10O5表示.
①产生N2的电极为电池的正极(填“正”或“负”).
②生成X(气体)的电极上发生的电极反应式为C6H10O5-24e-+7H2O═6CO2↑+24H+.
3.煤作为燃料有两种途径:
Ⅰ.C(s)+O2(g)═CO2(g)△H1<0
Ⅱ.C(s)+H2O(g)═CO(g)+H2(g)△H2>0
2CO(g)+O2(g)=2CO2(g△H3<0
2H2(g)+O2(g)═2H2O(g)△H4<0请回答:
(1)途径Ⅰ放出的热量=途径Ⅱ放出的热量(填“>”、“<”或“=”).
(2)△H1、△H2、△H3、△H4之间关系的数学表达式是△H1=△H2+$\frac{1}{2}$(△H3+△H4)
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表所示:
试回答下列问题:
①在一个温度恒定固定容积的密闭容器中发生上述反应,反应达到平衡的标志是cd
(填序号)
a.体系的压强不再改变 b.体系的密度不再改变 c.各气体的浓度不再改变
d.各气体的质量分数不再改变 e.反应速率v(CO):v(H2)=1:1
②上述反应的正反应是放热反应(填“放热”或“吸热”);
400℃时反应H2(g)+CO2(g)?CO(g)+H2O(g)的化学平衡常数数值是0.1;
③830℃时,在2L的密闭容器中加入4mol CO(g)和6mol H2O(g)发生反应,10分钟达到平衡,此10分钟内用H2表示的平均反应速率是0.12mol/(L•min);达到平衡时CO的转化率是60%.
(4)汽车尾气净化中的一个反应如:
NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.4kJ/mol
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是C

Ⅰ.C(s)+O2(g)═CO2(g)△H1<0
Ⅱ.C(s)+H2O(g)═CO(g)+H2(g)△H2>0
2CO(g)+O2(g)=2CO2(g△H3<0
2H2(g)+O2(g)═2H2O(g)△H4<0请回答:
(1)途径Ⅰ放出的热量=途径Ⅱ放出的热量(填“>”、“<”或“=”).
(2)△H1、△H2、△H3、△H4之间关系的数学表达式是△H1=△H2+$\frac{1}{2}$(△H3+△H4)
(3)煤化工中常需研究不同温度下平衡常数、投料比及产率等问题.
已知CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如表所示:
| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
①在一个温度恒定固定容积的密闭容器中发生上述反应,反应达到平衡的标志是cd
(填序号)
a.体系的压强不再改变 b.体系的密度不再改变 c.各气体的浓度不再改变
d.各气体的质量分数不再改变 e.反应速率v(CO):v(H2)=1:1
②上述反应的正反应是放热反应(填“放热”或“吸热”);
400℃时反应H2(g)+CO2(g)?CO(g)+H2O(g)的化学平衡常数数值是0.1;
③830℃时,在2L的密闭容器中加入4mol CO(g)和6mol H2O(g)发生反应,10分钟达到平衡,此10分钟内用H2表示的平均反应速率是0.12mol/(L•min);达到平衡时CO的转化率是60%.
(4)汽车尾气净化中的一个反应如:
NO(g)+CO(g)?$\frac{1}{2}$N2(g)+CO2(g)△H=-373.4kJ/mol
在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是C

1.在10L恒容密闭容器中充入X(g)和Y(g),发生反应X(g)+Y(g)?M(g)+N(g)△H,所得实验数据如下表.
(1)实验①中,若5min时测得n(M)=0.050mol,则0至5min时间内,v(N)=0.001mol/(L•min);
(2)实验②中,该反应的平衡常数K=1;
(3)实验③中,此时化学反应速率是v(正)<v(逆)(填“=”、“>”或“<”);
(4)反应热△H<0(填“>”或“<”);
(5)应用化学反应速率与化学平衡原理解决化工生产实际问题,你认为下列说法不正确的是c(填字母序号).
a.化学反应速率理论可以指导怎样在一定时间内快出产品
b.勒夏特列原理可以指导怎样使有限原料多出产品
c.催化剂的使用是提高产品产率的有效办法
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益.
| 实验 | 温度/℃ | 起始时物质的量/mol | 平衡时物质的量/mol | |||
| n(X) | n(Y) | n(M) | n(N) | n(M) | ||
| ① | 700 | 0.40 | 0.10 | 0 | 0 | 0.090 |
| ② | 800 | 0.10 | 0.40 | 0 | 0 | 0.080 |
| ③ | 800 | 0.20 | 0.30 | 0.25 | 0.25 | a |
(2)实验②中,该反应的平衡常数K=1;
(3)实验③中,此时化学反应速率是v(正)<v(逆)(填“=”、“>”或“<”);
(4)反应热△H<0(填“>”或“<”);
(5)应用化学反应速率与化学平衡原理解决化工生产实际问题,你认为下列说法不正确的是c(填字母序号).
a.化学反应速率理论可以指导怎样在一定时间内快出产品
b.勒夏特列原理可以指导怎样使有限原料多出产品
c.催化剂的使用是提高产品产率的有效办法
d.正确利用化学反应速率和化学反应限度都可以提高化工生产的综合经济效益.
9.某兴趣小组根据镁与沸水的反应推测镁也能与饱和碳酸氢钠溶液反应.资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.该兴趣小组设计了如下实验方案验证产物并探究反应原理.
实验1:用砂纸擦去镁条表面氧化膜,将其放人盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红.
(1)提出假设
该同学对反应中产生的白色不溶物作出如下假设:
假设1:可能为Mg(OH)2.
假设2:可能为MgCO3.
假设3:可能是碱式碳酸镁[xMgCO3•yMg(OH)2]
(2)设计定性实验确定产物并验证猜测:
(3)设计定量实验确定实验I的产物:称取实验Ⅰ中所得干燥、纯净的白色不溶物6.20g,充分加热灼烧至不再产生气体为止,并使分解产生的气体全部进入装置A(盛足量浓硫酸)和B(盛足量碱石灰)中.实验前后装置A增重0.36g,装置B增重2.64g,则白色不溶物的化学式3MgCO3•Mg(OH)2或Mg4(OH)2(CO3)3.
0 160563 160571 160577 160581 160587 160589 160593 160599 160601 160607 160613 160617 160619 160623 160629 160631 160637 160641 160643 160647 160649 160653 160655 160657 160658 160659 160661 160662 160663 160665 160667 160671 160673 160677 160679 160683 160689 160691 160697 160701 160703 160707 160713 160719 160721 160727 160731 160733 160739 160743 160749 160757 203614
实验1:用砂纸擦去镁条表面氧化膜,将其放人盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红.
(1)提出假设
该同学对反应中产生的白色不溶物作出如下假设:
假设1:可能为Mg(OH)2.
假设2:可能为MgCO3.
假设3:可能是碱式碳酸镁[xMgCO3•yMg(OH)2]
(2)设计定性实验确定产物并验证猜测:
| 实验序号 | 实验 | 预期现象和结论 |
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰①该气体为氢气 |
| 实验Ⅲ | 取实验I中的白色不溶物,洗涤,加入足量此空删去②稀盐酸 | 产生气泡,沉淀全部溶解;白色不溶物可能含有MgCO3 |
| 实验Ⅳ | 取实验I中的澄清液,向其中加入少量CaCl2溶液 | 产生白色沉淀;溶液中存在此空删去③CO32-离子 |



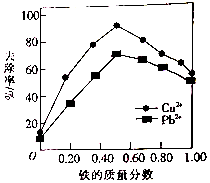 铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物.在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示.已知活性炭对重金属离子具有一定的吸附作用.
铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物.在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图所示.已知活性炭对重金属离子具有一定的吸附作用.