11.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2O所含原子个数大于3NA | |
| B. | 100ml18.4mol/L硫酸与足量Cu反应,生成SO2的分子数为0.92NA | |
| C. | t℃时,MgCO3的Ksp=4×10-6,则饱和溶液中含Mg2+数目为2×10-3NA | |
| D. | 100g质量分数为34.2%的蔗糖分子水溶液中含H原子数为2.2NA |
9.实验室里需要480mL0.100mol/LCuSO4溶液,以下配制操作正确的是( )
| A. | 称取7.68gCuSO4加水配成480mL溶液 | |
| B. | 称取12.5g 胆矾,加水配成500mL溶液 | |
| C. | 称取8.0CuSO4,加水500mL 溶解配成溶液 | |
| D. | 称取12.0g胆矾,加水480mL溶解配成溶液 |
8.实验是化学研究的基础,关于下列各实验装置图的叙述中,正确的是( )
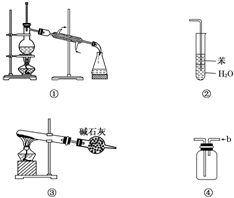

| A. | 装置①常用于分离互不相溶的液体混合物 | |
| B. | 装置②可用于吸收氨气,能够防止倒吸 | |
| C. | 以NH4HCO3为原料,装置③可用于制备少量CO2 | |
| D. | 装置④a口进气可收集Cl2、NO2等气体 |
7.在天平两边的托盘上各放一只等质量的烧杯,烧杯中各盛放等质量、等浓度的稀硫酸,向两烧杯中分别放入一块铁片和铝片(均与硫酸完全反应),天平仍然平衡.则放入的铁片和铝片的物质的量之比是( )
| A. | 1:1 | B. | 1:3 | C. | 2:3 | D. | 4:9 |
6.将1.85g含锌、铁、铜的合金放入足量的盐酸中,反应完毕后,得448mL(标况)氢气,关于此合金的组成,下列说法中不正确的是( )
| A. | 合金中铁、锌的物质的量之和为0.02mol | |
| B. | 合金中铜的质量无法确定 | |
| C. | 合金中铁、铜的物质的量之和为0.01mol | |
| D. | 1.30g>铁和锌质量之和>1.12g |
5.下列物质必须隔绝空气密封保存的是( )
①Na ②镁条 ③石灰水④NaOH ⑤Na2CO3•10H2O ⑥NaCl.
①Na ②镁条 ③石灰水④NaOH ⑤Na2CO3•10H2O ⑥NaCl.
| A. | ①② | B. | ①③④⑤ | C. | ①②③④ | D. | ①②①②④⑤ |
4.T1℃时,向容积为2L的密闭容器中充入一定量的A气体和B气体,发生如下反应:A(g)+2B(g)?C(g)
反应过程中测定的部分数据见表:下列说法正确的是( )
反应过程中测定的部分数据见表:下列说法正确的是( )
| 反应时间/min | n(A)/mol | n(B)/mol |
| 0 | 1.00 | 1.20 |
| 10 | 0.50 | |
| 30 | 0.20 |
| A. | 前10min内反应的平均速率为v(C)=0.050mol•L-1•min-1 | |
| B. | 保持其他条件不变,起始时向容器中充入0.50molA气体和0.60molB气体,到达平衡时,n(C)<0.25mol | |
| C. | 若密闭容器体积不变,其他条件不变,在达到平衡后持续缩小容器体积,则平衡一直会正向移动 | |
| D. | 温度为T2℃时(T1>T2),上述反应平衡常数为20,则正反应为放热反应 |
3.已知常温下0.1mol/L的NH4HCO3溶液pH=7.8,已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法不正确的是( )

0 160540 160548 160554 160558 160564 160566 160570 160576 160578 160584 160590 160594 160596 160600 160606 160608 160614 160618 160620 160624 160626 160630 160632 160634 160635 160636 160638 160639 160640 160642 160644 160648 160650 160654 160656 160660 160666 160668 160674 160678 160680 160684 160690 160696 160698 160704 160708 160710 160716 160720 160726 160734 203614

| A. | 溶液的pH=9时,溶液中存在下列关系:c(HCO3-)>c(NH4+)>c(NH3•H2O)>c(CO32-) | |
| B. | NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3•H2O)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | 由图可知,往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3-浓度逐渐减小 | |
| D. | 通过分析可知常温下Ka1(H2CO3)>Kb(NH3•H2O)>Ka2(H2CO3) |

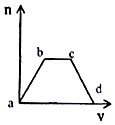 将足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的质量(m)和通入CO2体积(V)的关系如图所示:
将足量CO2通入KOH和Ca(OH)2的混合溶液中,生成沉淀的质量(m)和通入CO2体积(V)的关系如图所示: