2.用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 1molN2所含有的原子数为NA | |
| B. | 标准状况下,22.4L水中含有的水分子数为NA | |
| C. | Na2O2和CO2的反应中,每有1molNa2O2参加反应转移电子数为2NA | |
| D. | 16 gO2分子和16 gO3分子所含的氧原子数目相等 |
1.某无色溶液中下列各组离子能大量共存的是( )
| A. | Fe3+、Ba2+、NO3-、Cl- | B. | K+、Na+、OH-、NO3- | ||
| C. | H+、Ag+、Cl-、SO42- | D. | Cu2+、Ca2+、SO42-、OH- |
20.下列各组物质,按化合物、单质、混合物的顺序排列的是( )
| A. | 烧碱、液态氧、碘酒 | B. | 硫磺、白磷、小苏打 | ||
| C. | 干冰、铁、氯化氢 | D. | 空气、氮气、氯水 |
19.光纤通信的光学纤维是由下列哪种物质经特殊工艺制成的( )
| A. | 碳 | B. | 二氧化硅 | C. | 铜 | D. | 硅 |
18.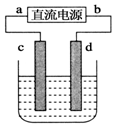 如图,电解质溶液是NaCl的水溶液,过一段时间发现d极附近有黄绿色气体产生,(c、d均为石墨电极)以下说法正确的是( )
如图,电解质溶液是NaCl的水溶液,过一段时间发现d极附近有黄绿色气体产生,(c、d均为石墨电极)以下说法正确的是( )
 如图,电解质溶液是NaCl的水溶液,过一段时间发现d极附近有黄绿色气体产生,(c、d均为石墨电极)以下说法正确的是( )
如图,电解质溶液是NaCl的水溶液,过一段时间发现d极附近有黄绿色气体产生,(c、d均为石墨电极)以下说法正确的是( )| A. | a是电源的正极 | B. | 电子流动的方向:d→b | ||
| C. | c极发生氧化反应 |
17.将两个铂电极插入KOH溶液中,向两极分别通入CH4和O2,即可构成CH4燃料电池.已知通入O2一极的电极反应式是:O2+2H2O+4e-═4OH-.下列有关叙述中,不正确的是( )
| A. | 通入CH4的电极为负极 | B. | 正极发生氧化反应 | ||
| C. | 溶液中的OH-向负极移动 | D. | 工作一段时间后应补充KOH |
16.向盛有10滴AgNO3溶液的试管中滴加0.1mol/L NaCl溶液,至不再有白色沉淀生成;继续向试管中滴加0.1mol/L KI溶液并振荡,沉淀变为黄色;再向试管中滴入0.1mol/L Na2S溶液并振荡,沉淀又变成黑色.根据上述变化过程,分析此三种沉淀物的溶解度关系为( )
| A. | AgCl=AgI=Ag2S | B. | AgCl<AgI<Ag2S | C. | AgCl>AgI>Ag2S | D. | AgI>AgCl>Ag2S |
15.相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HClO说法正确的是( )
| A. | 电离程度:HCN>HClO | |
| B. | pH:HClO>HCN | |
| C. | 酸根离子浓度:c(CN-)<c(ClO-) | |
| D. | 与NaOH溶液恰好完全反应时,消耗NaOH的物质的量:HClO>HCN |
14.某羧酸酯的分子式为C18H26O5,1mol该酯完全水解可得到1mol羧酸和2mol乙醇,该羧酸的分子式为( )
| A. | C16H22O5 | B. | C14H16O4 | C. | C14H18O5 | D. | C14H20O5 |
13.诺贝尔化学奖获得者施罗克等人发现金属钼的卡宾化合物可以作为非常有效的烯烃复分解催化剂.利用H2、CO和铝分别还原等量的MoO3,所消耗还原剂的物质的量之比为( )
0 160486 160494 160500 160504 160510 160512 160516 160522 160524 160530 160536 160540 160542 160546 160552 160554 160560 160564 160566 160570 160572 160576 160578 160580 160581 160582 160584 160585 160586 160588 160590 160594 160596 160600 160602 160606 160612 160614 160620 160624 160626 160630 160636 160642 160644 160650 160654 160656 160662 160666 160672 160680 203614
| A. | 3:3:2 | B. | 2:2:3 | C. | 3:28:27 | D. | 1:1:1 |