3.下列关于化学基本概念和基本理论的几点认识中正确的是( )
| A. | 胶体区别于其它分散系的本质特征是具有丁达尔现象 | |
| B. | 碱性氧化物一定是金属氧化物,金属氧化物不一定是碱性氧化物 | |
| C. | 根据化合物中含氢数目的多少,把化合物分为一元酸、二元酸、三元酸等 | |
| D. | 强电解质溶液的导电能力一定强于弱电解质溶液 |
2.下列物质的提纯(括号内为杂质),所选试剂和仪器正确的组合是( )
①Fe2O3(Al2O3):盐酸 ②H2O(I2):酒精 ③Na2CO3(NaHCO3):石灰水 ④豆油(水):不需试剂

①Fe2O3(Al2O3):盐酸 ②H2O(I2):酒精 ③Na2CO3(NaHCO3):石灰水 ④豆油(水):不需试剂

| A. | ①Ⅰ | B. | ②Ⅱ | C. | ③Ⅲ | D. | ④Ⅱ |
18.常温下,将一定量的钠铝合金置于水中,合金全部溶解,得到20mL pH=14的溶液,然后用1mol/L的盐酸滴定,测得生成沉淀的质量与消耗盐酸的体积关系如图所示,则下列说法正确的是( )
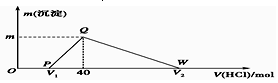

| A. | 原合金质量为0.92 g | |
| B. | 图中V2为60 | |
| C. | 整个滴定过程中Na+的浓度保持不变 | |
| D. | OP段发生的反应为:NaOH+HCl═NaCl+H2O |
17.强酸和强碱的稀溶液的中和热可表示为:H+(aq)+OH-(aq)═H2O(1);△H=-57.3kJ/mol.已知:
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(1);△H=-Q1kJ/mol
$\frac{1}{2}$H2SO4(浓)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(1);△H=-Q2kJ/mol
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(1);△H=-Q3kJ/mol
则Q1、Q2、Q3的关系正确的是( )
CH3COOH(aq)+NaOH(aq)═CH3COONa(aq)+H2O(1);△H=-Q1kJ/mol
$\frac{1}{2}$H2SO4(浓)+NaOH(aq)═$\frac{1}{2}$Na2SO4(aq)+H2O(1);△H=-Q2kJ/mol
HNO3(aq)+NaOH(aq)═NaNO3(aq)+H2O(1);△H=-Q3kJ/mol
则Q1、Q2、Q3的关系正确的是( )
| A. | Q3>Q2>Q1 | B. | Q1>Q3>Q2 | C. | Q1=Q2=Q3 | D. | Q2>Q3>Q1 |
16.用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 1.0mol.L-1的氨水中NH4+、NH3和NH3•H2O的总数为NA | |
| B. | 1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA | |
| C. | 0.1 mol Cu与足量浓硫酸反应生成SO2的体积约为4.48 L | |
| D. | 常温常压下,21g氧气和27 g臭氧所含的氧原子总数为3NA |
15.下列除杂质的操作方法不正确的是( )
| A. | 三氧化二铁中有少量的氧化铝:加过量的烧碱溶液后过滤洗涤 | |
| B. | 氯化钠中有少量的I2:通过加热的方法 | |
| C. | CO中有少量的CO2:用氢氧化钠洗涤后再干燥 | |
| D. | 食盐中有少量的氧化铝:加过量的烧碱溶液后蒸发结晶 |
14.只用一种试剂就能将Na2SiO3、Na2CO3、MgCl2、Ba(HCO3)2四种无色溶液区别开来,这种试剂是( )
0 160474 160482 160488 160492 160498 160500 160504 160510 160512 160518 160524 160528 160530 160534 160540 160542 160548 160552 160554 160558 160560 160564 160566 160568 160569 160570 160572 160573 160574 160576 160578 160582 160584 160588 160590 160594 160600 160602 160608 160612 160614 160618 160624 160630 160632 160638 160642 160644 160650 160654 160660 160668 203614
| A. | 氢氧化钠溶液 | B. | 澄清石灰水 | C. | 2 mol/L 盐酸 | D. | 2 mol/L 硫酸 |




