12.如表中实验“操作和现象”与“结论或目的一均正确的一组是( )
| 操作和现象 | 结论或目的 | |
| A | 向纯碱中滴加足量浓盐酸,将所得气体通入硅酸钠溶液中,溶液变浑浊 | 酸性:盐酸>碳酸>苯酚 |
| B | 取某溶液少量,加入盐酸酸化的氯化钡溶液,出现白色沉淀 | 该溶液中一定含有大量的SO42- |
| C | 取少量Fe(NO3)2试样加水溶液后加稀硫酸酸化,滴加KSCN溶液,溶液变为红色 | 该Fe(NO3)2试样已经变质 |
| D | 处理锅炉水垢中的CaSO4时,依次加入饱和Na2CO3溶液和盐酸,水垢溶解 | 目的:将不溶于酸的沉淀转化为易溶于酸的沉淀 |
| A. | A | B. | B | C. | C | D. | D |
11.化学与科学、技术、社会、环境密切相关.下列说法不正确的是( )
| A. | 聚乙烯是无毒高分子化合物,可用作食品包装 | |
| B. | 人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外 | |
| C. | “地沟油”经过加工处理后,可以用来制肥皂和生物柴油 | |
| D. | 电子垃圾的回收利用,可减少对土壤和水源的污染 |
8.下列叙述中不正确的是( )
| A. | 常温时,某溶液中由水电离出来的c(H+)和c(OH-)的乘积为l×10-24,该溶液中一定可以大量存在K+、Na+、AlO-2、SO2-4 | |
| B. | 1 mol Na2O和Na2O2混合物中含有的阴、阳离子总数是3NA | |
| C. | 镍镉可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2$?_{放电}^{充电}$Cd(OH)2+2Ni(OH)2+2H2O,充电时阳极反应为:Ni(OH)2+OH-+e-═NiO(OH)+H2O | |
| D. | 某一反应体系中的物质有:HCl、SnCl2、H2SnCl6、As、H3AsO3、H2O.已知As是产物之一,则该反应配平后H2O的化学计量数为6 |
7.下列说法不正确的是( )
| A. | 一定温度下,某密闭容器发生如下反应:CaCO3(s)?CaO(s)+CO2(g),达到平衡后,将容器体积缩小为原来的一半,当体系再次达到化学平衡时,CO2的物质的量浓度不变 | |
| B. | 已知某温度下,Kw=l×10-13,若将pH=8的NaOH溶液与pH=5的H2SO4溶液混合,保持温度不变,欲使混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为11:9 | |
| C. | 已知:KSP(AgCl)=1.8×10-10,Ksp(Ag2CrO2)=2.0×10-12,将0.001 mol•L-1的AgNO3溶液滴入0.001mol•L-1 KCl和0.001 rnol•L-1IK2CrO4的混合溶液中,先产生AgCl沉淀 | |
| D. | 已知25℃时,有关弱酸的电离平衡常数:HCNKa=4.9×10-10:H2CO3,Ka1=4.3×10-7,Ka2=5.6×10-11.则CO2通入NaCN溶液中反应的化学方程式为:2NaCN+H2O+CO2═2HCN+Na2CO3 |
6.下列说法不正确的是( )
| A. | 纸层析法中的展开剂之所以能够展开的主要原理是毛细现象 | |
| B. | 在中和滴定实验中,既可用标准溶液滴定待测液,也可用待测液滴定标准溶液 | |
| C. | 实验中需用2.0 mol•L-1的Na2 CO3溶液950 mL,配制时应选用的容量瓶的规格和称取Na2CO3的质量分别为950mL,201.4g | |
| D. | 减压过滤的原理是抽气泵给吸滤瓶减压,造成吸滤瓶内与布氏漏斗液面上的压力差,从而加快过滤速度 |
5.下列说法正确的是( )
| A. | 水晶、玛瑙、红宝石、蓝宝石的主要成分都是非金属氧化物 | |
| B. | 蛋白质是结构复杂的高分子化合物,蛋白质的生物活性首先取决于蛋白质的一级结构 | |
| C. | 同位素示踪法是研究化学反应历程的手段之一,红外光谱法可用于研究有机物分子结构,滴定法不能用于测量盐类物质溶液的浓度 | |
| D. | 丁达尔现象可用于区别溶液与胶体,云、雾、稀硫酸均能产生丁达尔现象 |
3.工业上合成氨的反应是:N2(g)+3H2(g)?2NH3(g)△H=-92.20kJ•mol-1.
(1)在绝热固定容积的密闭容器发生反应:N2(g)+3H2(g)?2NH3(g),能说明上述反应向正反应方向移动的是②④
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N-H的同时生成2n mol H-H
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
④混合气体的平均摩尔质量增大
⑤容器内气体密度不变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
根据表中数据计算:
①反应进行到2小时时放出的热量为27.78KJ
②0~l小时内N2的平均反应速率0.05mol•L-1•h-1;
③此条件下该反应的化学平衡常数K=0.15(保留两位小数)
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向正反应方向移动(填“正反应”、“逆反应”或“不移动”).
0 160433 160441 160447 160451 160457 160459 160463 160469 160471 160477 160483 160487 160489 160493 160499 160501 160507 160511 160513 160517 160519 160523 160525 160527 160528 160529 160531 160532 160533 160535 160537 160541 160543 160547 160549 160553 160559 160561 160567 160571 160573 160577 160583 160589 160591 160597 160601 160603 160609 160613 160619 160627 203614
(1)在绝热固定容积的密闭容器发生反应:N2(g)+3H2(g)?2NH3(g),能说明上述反应向正反应方向移动的是②④
①单位时间内生成2n mol NH3的同时生成3n mol H2
②单位时间内生成6n mol N-H的同时生成2n mol H-H
③用N2、H2、NH3的物质的量浓度变化表示的反应速率之比为1:3:2
④混合气体的平均摩尔质量增大
⑤容器内气体密度不变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
| 时间(h) 物质的量(mol) | 0 | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0 | 0.20 | 1.00 | 1.00 |
①反应进行到2小时时放出的热量为27.78KJ
②0~l小时内N2的平均反应速率0.05mol•L-1•h-1;
③此条件下该反应的化学平衡常数K=0.15(保留两位小数)
④反应达到平衡后,若往平衡体系中再加入N2、H2和NH3各1.00mol,化学平衡将向正反应方向移动(填“正反应”、“逆反应”或“不移动”).



 .
. .
. .
.

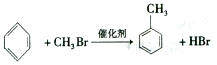 ;②C物质苯环上一卤代物只有两种.
;②C物质苯环上一卤代物只有两种. .
. $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$
 +
+
 .
.