11.下列实验操作或事故处理正确的是( )
| A. | 实验室中酒精灯着火,立即用水扑灭 | |
| B. | 实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室 | |
| C. | 皮肤上不慎沾上NaOH溶液,立即用盐酸冲洗 | |
| D. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 |
10.设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,2.24 L水中含有的分子数约为0.l NA | |
| B. | 在常温常压下,1 mol He含有的原子数为NA | |
| C. | 2.4g金属镁变为镁离子时失去的电子数为0.1NA | |
| D. | 物质的量浓度为0.5mol/L FeCl3溶液中Cl-的数目为1.5NA |
9.已知:t℃下的某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为:K=$\frac{c(X)•{c}^{2}(Y)}{{c}^{2}(Z)•{c}^{2}(W)}$,有关该平衡的说法中正确的是( )
| A. | 升高温度,平衡常数K变大 | |
| B. | 增大压强,W(g)物质的量分数变大 | |
| C. | 升温,若混合气体的平均相对分子质量变小,则正反应放热 | |
| D. | 增大X浓度,平衡向正反应方向移动 |
7.氨是一种重要的化工产品,是氮肥工业、有机合成工业以及制造硝酸、铵盐和纯碱等的原料.
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3 该可逆反应达到平衡的标志是BCE.
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间而变化
E.a mol N≡N键断裂的同时,有6a mol N-H键断裂
F.N2、H2、NH3的分子数之比为1:3:2
(2)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如表:
则从反应开始到25min时,以N2表示的平均反应速率=0.01 mol/(L•min);
该温度下平衡常数K=2.37.
(1)在一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3 该可逆反应达到平衡的标志是BCE.
A.3v(H2)正=2v(NH3)逆
B.单位时间生成m mol N2的同时消耗3m mol H2
C.容器内的总压强不再随时间而变化
D.混合气体的密度不再随时间而变化
E.a mol N≡N键断裂的同时,有6a mol N-H键断裂
F.N2、H2、NH3的分子数之比为1:3:2
(2)某化学研究性学习小组模拟工业合成氨的反应.在容积固定为2L的密闭容器内充入1mol N2和3mol H2,加入合适催化剂(体积可以忽略不计)后在一定温度压强下开始反应,并用压力计监测容器内压强的变化如表:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| 压强/MPa | 16.80 | 14.78 | 13.86 | 13.27 | 12.85 | 12.60 | 12.60 |
该温度下平衡常数K=2.37.
6.下列实验事实能用勒夏特烈原理解释的是( )
| A. | 夏天打开啤酒盖,喷出大量泡沫 | |
| B. | 工业上合成氨气时采用高温利于氨气的合成 | |
| C. | 在HI的分解实验达到平衡后加压颜色变深 | |
| D. | 锌和稀硫酸制备氢气时滴入少量硫酸铜可以加快速率 |
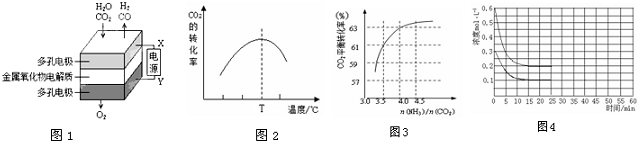
5.Na2SO3的氧化反应:2Na2SO3(aq)+O2(aq)=2Na2SO4(aq)△H=m kJ•mol-1.其反应速率受溶解氧浓度影响,分为富氧区和贫氧区两个阶段.
(1)已知O2(g)?O2(aq)△H=nkJ•mol-1,Na2SO3溶液与O2(g)反应的热化学方程式为2Na2SO3(aq)+O2(g)=2Na2SO4(aq)△H=(m+n)kJ•mol-1
(2)291.5K时,1.0L溶液中Na2SO3初始量分别为4、6、8、12mmol,溶解氧浓度初始值为9.60mg•L-1,每5s记录溶解氧浓度,实验结果如图.当Na2SO3的初始量为12mmol,经过20s溶解氧浓度降为6.40mg•L-1,则0-20s内Na2SO3的平均反应速率为1.00×10-5mol•L-1•s-1
(3)为确定贫氧区速率方程v=kca(SO32-)•cb(O2)中a,b的值(取整数),分析实验数据.
①当溶解氧浓度为4.0mg•L-1时,c(Na2SO3)与速率数值关系如表,则a=2
②当溶解氧浓度小于4.0mg•L-1时,图中曲线皆为直线,则b=0,
(4)两个阶段不同温度的速率常数(k)之比如表.
已知ln$\frac{{k}_{2}}{{k}_{1}}$=-$\frac{{E}_{a}}{R}$($\frac{1}{{T}_{2}}-\frac{1}{{T}_{1}}$),R为常数,Ea(富氧区)<Ea(贫氧区)(填“>”或“<”).
(5)结合图表分析,Na2SO3初始量不同时,划分富氧区与贫氧区的溶解氧浓度是否相同,为什么?.
(6)一定温度下,化学反应速率仅与决速步的反应物浓度有关.Na2SO3氧化反应历程涉及的
①SO32-+O2→SO5-
②SO5-+SO32-→SO52-+SO3-
③SO32-+SO32-→SO3-+SO32-
④SO32-+O2→SO5-
⑤SO52-+SO32-→2SO42-
富氧区与和贫氧区的决速步分别是①、③(填序号)
(1)已知O2(g)?O2(aq)△H=nkJ•mol-1,Na2SO3溶液与O2(g)反应的热化学方程式为2Na2SO3(aq)+O2(g)=2Na2SO4(aq)△H=(m+n)kJ•mol-1
(2)291.5K时,1.0L溶液中Na2SO3初始量分别为4、6、8、12mmol,溶解氧浓度初始值为9.60mg•L-1,每5s记录溶解氧浓度,实验结果如图.当Na2SO3的初始量为12mmol,经过20s溶解氧浓度降为6.40mg•L-1,则0-20s内Na2SO3的平均反应速率为1.00×10-5mol•L-1•s-1
(3)为确定贫氧区速率方程v=kca(SO32-)•cb(O2)中a,b的值(取整数),分析实验数据.
| c(Na2SO3)×103 | 3.65 | 5.65 | 7.65 | 11.65 |
| v×106 | 10.2 | 24.4 | 44.7 | 103.6 |

②当溶解氧浓度小于4.0mg•L-1时,图中曲线皆为直线,则b=0,
(4)两个阶段不同温度的速率常数(k)之比如表.
| 反应阶段 | 速率方程 | $\frac{k(297.0K)}{k(291.5K)}$ |
| 富氧区 | v=kc(SO32-)•c(O2) | 1.47 |
| 贫氧区 | v=kca(SO32-)•cb(O2) | 2.59 |
(5)结合图表分析,Na2SO3初始量不同时,划分富氧区与贫氧区的溶解氧浓度是否相同,为什么?.
(6)一定温度下,化学反应速率仅与决速步的反应物浓度有关.Na2SO3氧化反应历程涉及的
①SO32-+O2→SO5-
②SO5-+SO32-→SO52-+SO3-
③SO32-+SO32-→SO3-+SO32-
④SO32-+O2→SO5-
⑤SO52-+SO32-→2SO42-
富氧区与和贫氧区的决速步分别是①、③(填序号)
4.在100℃时,将0.100mol的N2O4气体充入1L抽空密闭容器中,发生反应:N2O4(g)?2NO2.
现在隔一定时间对该容器内的物质进行分析,得到如下表格:
试回答下列问题:
(1)达到平衡时N2O4的转化率为60%,表中c2>c3,a=b(后两空选填>、<、=)
(2)20s的N2O4的浓度c1=0.07mol/L在0~20s内N2O4的平均反应速率为0.0015mol/(L•s);
(3)若其他反应条件以及初始物质物质的量不变,将反应的温度降低到80℃时,达到平衡时NO2的物质的量为0.100mol,那么正反应是吸热反应(选填吸热或放热)
(4)若在相同初始情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度为0.20mol/L.
0 160421 160429 160435 160439 160445 160447 160451 160457 160459 160465 160471 160475 160477 160481 160487 160489 160495 160499 160501 160505 160507 160511 160513 160515 160516 160517 160519 160520 160521 160523 160525 160529 160531 160535 160537 160541 160547 160549 160555 160559 160561 160565 160571 160577 160579 160585 160589 160591 160597 160601 160607 160615 203614
现在隔一定时间对该容器内的物质进行分析,得到如下表格:
| t/s c/(mol•L-1) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)/(mol•L-1) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/(mol•L-1) | 0 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)达到平衡时N2O4的转化率为60%,表中c2>c3,a=b(后两空选填>、<、=)
(2)20s的N2O4的浓度c1=0.07mol/L在0~20s内N2O4的平均反应速率为0.0015mol/(L•s);
(3)若其他反应条件以及初始物质物质的量不变,将反应的温度降低到80℃时,达到平衡时NO2的物质的量为0.100mol,那么正反应是吸热反应(选填吸热或放热)
(4)若在相同初始情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度为0.20mol/L.
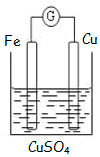 如图为牺牲阳极的阴极保护法的实验装置,此装置中Zn电极上的电极反应为Zn-2e-=Zn2+;如果将Zn换成Pt,一段时间后,在铁电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液时,烧杯中的现象是产生蓝色沉淀,发生的反应的离子方程式是3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓.
如图为牺牲阳极的阴极保护法的实验装置,此装置中Zn电极上的电极反应为Zn-2e-=Zn2+;如果将Zn换成Pt,一段时间后,在铁电极区滴入2滴黄色K3[Fe(CN)6](铁氰化钾)溶液时,烧杯中的现象是产生蓝色沉淀,发生的反应的离子方程式是3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓. (1)已知如图所示的可逆反应:
(1)已知如图所示的可逆反应: