2.汽车尾气排放的一氧化碳、氮氧化物等气体已成为大气污染的主要来源.德国大众汽车尾气检测造假事件引起全世界震惊.同时能源又是制约国家发展进程的因素之一.甲醇、二甲醚等被称为21世纪的绿色能源,工业上可利用天然气为主要原料与二氧化碳、水蒸气在一定条件下制备合成气(CO、H2),再制成甲醇、二甲醚.
请根据如图1示意图回答(1)、(2)有关问题:
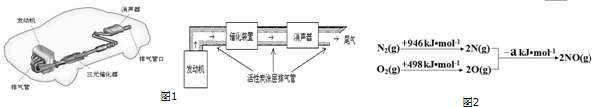
(1)汽车发动机工作时会引发N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1,其能量变化示意图如图2:
则NO中氮氧键的键能为632 kJ•mol-1.
(2)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口 C.升高排气管温度 D.添加合适的催化剂
(3)工业上一般采用下列两种反应合成甲醇:
反应a:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.5kJ•mol-1
反应b:CO (g)+2H2(g)?CH3OH(g)△H=-91.8kJ•mol-1
①对于反应a,某温度下,将4.0mol CO2(g)和12.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,测得甲醇蒸气的体积分数为30%,则该温度下反应的平衡常数为1.33;
②对于反应b,在763K、3.04×104kPa时,用CO和H2做原料合成CH3OH,当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响.设H2和CO起始物质的量之比为m,平衡时CO的转化率为α,平衡混合物中甲醇的体积分数为y,则m、α、y三者的关系式为y=$\frac{α}{1+m+2a}$
(i)请根据上述关系式将如表空白填满:
(ii)根据表中提供的数据,可得出反应物的比例对CO转化率以及平衡混合物中甲醇的体积分数影响的结论.选择最佳反应物配比是m=2,α=0.45;理由是由表中数据可知,m越大,α越大; 开始时m增大,y也随着增大,当m>2时,m增大,y减小,当m=2时,y最大 .
(4)CO可以合成二甲醚,二甲醚可以作为燃料电池的原料,化学反应原理为:
CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H<0
①在恒容密闭容器里按体积比为1:4充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是D;
A.逆反应速率先增大后减小
B.通入一定量的He,体系压强增大
C.正反应速率先减小后增大
D.化学平衡常数K值增大
②已知参与电极反应的电极材料单位质量放出电能的大小称为该电池的比能量.关于二甲醚碱性燃料电池与乙醇碱性燃料电池,下列说法正确的是AC(填字母)
A.两种燃料互为同分异构体,分子式和摩尔质量相同,但比能量不相同
B.两种燃料所含共价键数目相同,断键时所需能量相同,比能量相同
C.两种燃料所含共价键类型不同,断键时所需能量不同,比能量不同
③已知甲醇的热值是23kJ•g-1,请写出表示甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-736kJ/mol.
请根据如图1示意图回答(1)、(2)有关问题:

(1)汽车发动机工作时会引发N2(g)+O2(g)═2NO(g)△H=+180kJ•mol-1,其能量变化示意图如图2:
则NO中氮氧键的键能为632 kJ•mol-1.
(2)利用活性炭涂层排气管处理NOx的反应为:xC(s)+2NOx(g)?N2(g)+xCO2 (g)△H=-b kJ•mol-1.若使NOx更加有效的转化为无毒尾气排放,以下措施理论上可行的是AD.
A.增加排气管长度 B.增大尾气排放口 C.升高排气管温度 D.添加合适的催化剂
(3)工业上一般采用下列两种反应合成甲醇:
反应a:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-49.5kJ•mol-1
反应b:CO (g)+2H2(g)?CH3OH(g)△H=-91.8kJ•mol-1
①对于反应a,某温度下,将4.0mol CO2(g)和12.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,测得甲醇蒸气的体积分数为30%,则该温度下反应的平衡常数为1.33;
②对于反应b,在763K、3.04×104kPa时,用CO和H2做原料合成CH3OH,当原料中CO和H2的比例不同时,对CO的转化率及平衡混合物中甲醇的体积分数都有影响.设H2和CO起始物质的量之比为m,平衡时CO的转化率为α,平衡混合物中甲醇的体积分数为y,则m、α、y三者的关系式为y=$\frac{α}{1+m+2a}$
(i)请根据上述关系式将如表空白填满:
| m | α | y |
| 1 | 0.25 | 16.67% |
| 2 | 0.45 | |
| 3 | 0.56 | 19.35% |
(4)CO可以合成二甲醚,二甲醚可以作为燃料电池的原料,化学反应原理为:
CO(g)+4H2(g)?CH3OCH3(g)+H2O(g)△H<0
①在恒容密闭容器里按体积比为1:4充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是D;
A.逆反应速率先增大后减小
B.通入一定量的He,体系压强增大
C.正反应速率先减小后增大
D.化学平衡常数K值增大
②已知参与电极反应的电极材料单位质量放出电能的大小称为该电池的比能量.关于二甲醚碱性燃料电池与乙醇碱性燃料电池,下列说法正确的是AC(填字母)
A.两种燃料互为同分异构体,分子式和摩尔质量相同,但比能量不相同
B.两种燃料所含共价键数目相同,断键时所需能量相同,比能量相同
C.两种燃料所含共价键类型不同,断键时所需能量不同,比能量不同
③已知甲醇的热值是23kJ•g-1,请写出表示甲醇燃烧热的热化学方程式CH3OH(g)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(l)△H=-736kJ/mol.
1. 碳氧化物研究
碳氧化物研究
(1)在体积可变 (活塞与容器之间的摩擦力忽略不计)的密闭容器如右图所示,现将3molH2和2molCO放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成甲醇的反应如下:CO(g)+2H2(g)═CH3OH(g),测定不同条件、不同时间段内的CO的转化率,得到如表数据:
①根据如表数据,请比较T1<T2(选填“>”、“<”或“=”);T2℃下,第30min 时,a1=50%,升高温度该反应的化学平衡常数减小(选填“增大”、“减小”、“不变”).
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)< v(逆)(选填“>”、“<”或“=”).
③现有以下几种情况放入该体积可变的密闭容器中,请选出T2℃下达到的平衡状态与①中T2℃下的平衡状态一致的是
A、2mol H2+1molCO+1molCH3OH
B、0.5mol H2+1.5molCH3OH
C、1mol H2+1molCO+1molCH3OH
D、2mol H2+4molCH3OH
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=$\frac{2b}{a-2b}$×10-7L/mol(用含a和b的代数式表示).
 碳氧化物研究
碳氧化物研究(1)在体积可变 (活塞与容器之间的摩擦力忽略不计)的密闭容器如右图所示,现将3molH2和2molCO放入容器中,移动活塞至体积V为2L,用铆钉固定在A、B点,发生合成甲醇的反应如下:CO(g)+2H2(g)═CH3OH(g),测定不同条件、不同时间段内的CO的转化率,得到如表数据:
| CO的转化率 T(℃) | 10min | 20min | 30min | 40min |
| T1 | 20% | 55% | 65% | 65% |
| T2 | 35% | 50% | a1 | a2 |
②T2℃下,第40min时,拔去铆钉(容器密封性良好)后,活塞没有发生移动,再向容器中通人6molCO,此时v(正)< v(逆)(选填“>”、“<”或“=”).
③现有以下几种情况放入该体积可变的密闭容器中,请选出T2℃下达到的平衡状态与①中T2℃下的平衡状态一致的是
A、2mol H2+1molCO+1molCH3OH
B、0.5mol H2+1.5molCH3OH
C、1mol H2+1molCO+1molCH3OH
D、2mol H2+4molCH3OH
(2)一定条件下可用甲醇与CO反应生成醋酸消除CO污染.常温下,将a mol/L的醋酸与b mol/L Ba(OH)2溶液等体积混合,充分反应后,溶液中存在2c(Ba2+)=c(CH3COO-),则该混合溶液中醋酸的电离常数Ka=$\frac{2b}{a-2b}$×10-7L/mol(用含a和b的代数式表示).
17.I.通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能.如表为一些化学键的键能数据
写出硅高温燃烧的热化学方程式Si(s)+O2(g)=SiO2(s)△H=(2a+b-4c)kJ/mol.
Ⅱ.利用太阳光分解水制氢是未来解决能源危机的理想方法之一.某研究小组设计了如图所示的循环系统实现光分解水制氢.反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用.

(1)写出下列反应池中反应的离子方程式:
电解池A2H++2I-=H2+I2.
电解池B4Fe3++2H2O=4Fe2++O2+4H+.
(2)若电解池A中生成3.36L H2(标准状况),计算电解池B中生成Fe2+的物质的量为0.3mol
Ⅲ.在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:

N2(g)+3H2(g) 2NH3(g);△H<0
反应达到平衡后,测得混合气体为7体积.
请据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同.
①a=1,c=2,则b=3.在此情况下,反应起始时将向逆反应方向(填“正”或“逆”)进行.
②若需规定起始时反应向逆方向进行,则c的取值范围是1<c≤4.
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是降低温度,原因是降低温度平衡向正反应方向移动,气体总分子数减少.
0 160420 160428 160434 160438 160444 160446 160450 160456 160458 160464 160470 160474 160476 160480 160486 160488 160494 160498 160500 160504 160506 160510 160512 160514 160515 160516 160518 160519 160520 160522 160524 160528 160530 160534 160536 160540 160546 160548 160554 160558 160560 160564 160570 160576 160578 160584 160588 160590 160596 160600 160606 160614 203614
| 化学键 | Si-Si | O=O | Si-O |
| 键能/kJ•mol-1 | a | b | c |
Ⅱ.利用太阳光分解水制氢是未来解决能源危机的理想方法之一.某研究小组设计了如图所示的循环系统实现光分解水制氢.反应过程中所需的电能由太阳能光电池提供,反应体系中I2和Fe3+等可循环使用.

(1)写出下列反应池中反应的离子方程式:
电解池A2H++2I-=H2+I2.
电解池B4Fe3++2H2O=4Fe2++O2+4H+.
(2)若电解池A中生成3.36L H2(标准状况),计算电解池B中生成Fe2+的物质的量为0.3mol
Ⅲ.在一定的温度下,把2体积N2和6体积H2分别通入一个带活塞的体积可变的容器中,活塞的一端与大气相通,容器中发生如下反应:

N2(g)+3H2(g) 2NH3(g);△H<0
反应达到平衡后,测得混合气体为7体积.
请据此回答下列问题:
(1)保持上述反应温度不变,设a、b、c分别表示加入的N2、H2和NH3的体积,如果反应达到平衡后混合气体中各物质的量仍与上述平衡时完全相同.
①a=1,c=2,则b=3.在此情况下,反应起始时将向逆反应方向(填“正”或“逆”)进行.
②若需规定起始时反应向逆方向进行,则c的取值范围是1<c≤4.
(2)在上述装置中,若需控制平衡后混合气体为6.5体积,则可采取的措施是降低温度,原因是降低温度平衡向正反应方向移动,气体总分子数减少.
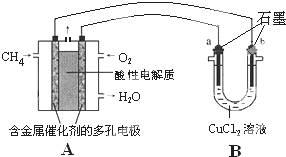 (3)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图.
(3)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解50mL 2mol/L的氯化铜溶液的装置示意图.
 据报道,一定条件下 Fe2O3可被甲烷还原为“纳米级”的金属铁.其反应为:Fe2O3(s)+3CH4(g)?2Fe(s)+3CO(g)+6H2(g)
据报道,一定条件下 Fe2O3可被甲烷还原为“纳米级”的金属铁.其反应为:Fe2O3(s)+3CH4(g)?2Fe(s)+3CO(g)+6H2(g)



 )的废水可以通过构成微生物电池除去,其原理如图5所示.
)的废水可以通过构成微生物电池除去,其原理如图5所示.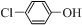 +2e-+H+═
+2e-+H+═ -OH+Cl-.
-OH+Cl-.