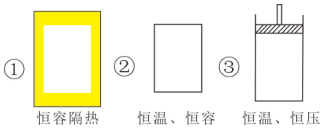
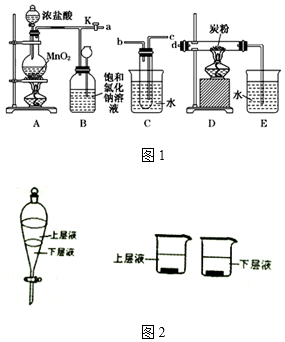
1.根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( )


| A. | t1时改变某一条件有如图所示变化,则改变的条件一定是加入催化剂 | |
| B. | 反应达到平衡时,外界条件对平衡影响关系如图所示,若b=1,a为正整数,则P1<P2 | |
| C. | 从加入反应物开始,物质的百分含量与温度关系如图所示,则该反应的正反应为吸热反应 | |
| D. | 反应速率和反应条件变化如图所示,则该反应正反应为放热反应,A、B一定是气体,D一定不是气体,C可能不是气体 |
20.在1200℃时,天然气脱硫工艺中会发生下列反应
H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H12H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2
2H2S(g)+O2(g)═2 S(g)+2H2O(g)△H32S(g)═S2(g)△H4
则△H4的正确表达式为( )
H2S(g)+$\frac{3}{2}$O2(g)═SO2(g)+H2O(g)△H12H2S(g)+SO2(g)═$\frac{3}{2}$S2(g)+2H2O(g)△H2
2H2S(g)+O2(g)═2 S(g)+2H2O(g)△H32S(g)═S2(g)△H4
则△H4的正确表达式为( )
| A. | △H4=$\frac{2}{3}$ (3△H3-△H1)-△H2 | B. | △H4=$\frac{2}{3}$ (△H1+△H2)+△H3 | ||
| C. | △H4=$\frac{2}{3}$ (△H1+△H2)-△H3 | D. | △H4=$\frac{2}{3}$ (△H1-△H2)-△H3 |
18.范德华力为a kJ•mol-1,化学键为b kJ•mol-1,氢键为c kJ•mol-1,则a、b、c的大小关系是( )
| A. | b>c>a | B. | b>a>c | C. | c>b>a | D. | a>b>c |
17.如图装置,将溶液A逐滴加入固体B中,下列叙述中不正确的是( )
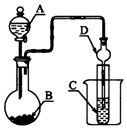

| A. | 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色 | |
| B. | 若A为醋酸溶液,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊 | |
| C. | 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液不褪色 | |
| D. | 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀 |
15.设NA为阿伏伽德罗常数的值.下列有关叙述正确的是( )
0 160417 160425 160431 160435 160441 160443 160447 160453 160455 160461 160467 160471 160473 160477 160483 160485 160491 160495 160497 160501 160503 160507 160509 160511 160512 160513 160515 160516 160517 160519 160521 160525 160527 160531 160533 160537 160543 160545 160551 160555 160557 160561 160567 160573 160575 160581 160585 160587 160593 160597 160603 160611 203614
| A. | 1molFe溶于过量硝酸,电子转移数为2NA | |
| B. | 1mol O2和2mol SO2反应生成的SO3分子数为2NA | |
| C. | 常温常压下,4.4gCO2与N2O混合气体中含有的原子数为0.3NA | |
| D. | H2O2分解产生1molO2,转移的电子数为4NA |
 (1)已知可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)△H
(1)已知可逆反应CO(g)+H2O(g)?CO2(g)+H2(g)△H