13.在酸性高锰酸钾溶液中加入Na2O2粉末,高锰酸钾溶液褪色,其中发生反应的离子方程式为:2MnO4-+16H++5Na2O2═2Mn2++5O2↑+8H2O+10Na+下列判断正确的是( )
| A. | 高锰酸钾是氧化剂,Na2O2既是氧化剂,又是还原剂 | |
| B. | 反应的氧化产物Mn2+ | |
| C. | 当反应产生标准状况下2.24L O2 时,反应转移的电子为0.2mol | |
| D. | 向高锰酸钾溶液滴加浓盐酸可以得到酸性高锰酸钾溶液 |
11.下列反应中,不属于四大基本反应类型,但属于氧化还原反应的是( )
| A. | 2Na+2H2O=2 NaOH+H2↑ | B. | Cl2+H2O=HCl+HClO | ||
| C. | CaCO3=CaO+CO2↑ | D. | Ca(ClO)2+2HCl=CaCl2+2HClO |
10.关于1.5mol NH3的说法错误的是( )
| A. | 摩尔质量为17 g•mol-1 | |
| B. | 所含的分子数目约为9.03×1023 | |
| C. | 在标准状况下体积约为33.6L | |
| D. | 溶于水制成0.5L溶液时物质的量浓度为1.5mol•L-1 |
7.常温下,在两份相同的 Ba(OH)2溶液中,分别滴入物质的量浓度相等的H2SO4、NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示.下列分析不正确的是( )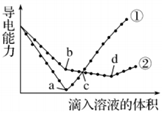

| A. | b点,水电离产生的c(H+)<10-7mol/L | B. | ①代表滴加H2SO4溶液的变化曲线 | ||
| C. | a、d两点对应的溶液均显中性 | D. | c点,两溶液中含有相同量的 OH- |
6.反应C(s)+H2O(g)?CO(g)+H2(g)在一可变容积的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是( )
①增加C的量
②保持体积不变,充入N2使体系压强增大
③将容器的体积缩小一半
④保持压强不变,充入N2使容器体积变大.
①增加C的量
②保持体积不变,充入N2使体系压强增大
③将容器的体积缩小一半
④保持压强不变,充入N2使容器体积变大.
| A. | ①④ | B. | ①② | C. | ②③ | D. | ②④ |
5.下面是四位同学在学习“化学反应的速率和化学平衡”一章后,联系工业生产实际所发表的观点,你认为不正确的是( )
0 160389 160397 160403 160407 160413 160415 160419 160425 160427 160433 160439 160443 160445 160449 160455 160457 160463 160467 160469 160473 160475 160479 160481 160483 160484 160485 160487 160488 160489 160491 160493 160497 160499 160503 160505 160509 160515 160517 160523 160527 160529 160533 160539 160545 160547 160553 160557 160559 160565 160569 160575 160583 203614
| A. | 使用催化剂,可加快反应速率,目的是提高生产效率 | |
| B. | 使用冰箱保存食物,是利用了化学反应速率理论 | |
| C. | 化学反应速率理论是研究怎样提高原料转化率 | |
| D. | 化学平衡理论是研究怎样使用有限原料多出产品 |
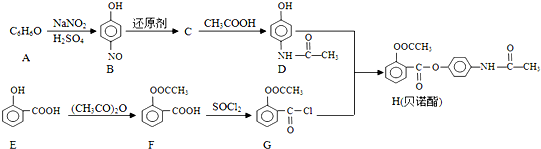
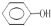 ;E中含氧官能团的名称为羟基、羧基.
;E中含氧官能团的名称为羟基、羧基.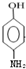 .
.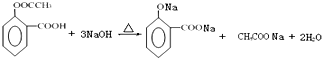 .
.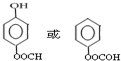 .
.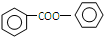 的合成路线流程图(无机试剂可任选):
的合成路线流程图(无机试剂可任选):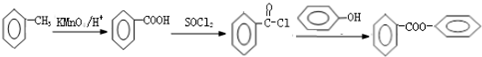 .
.