4.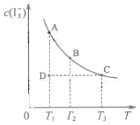 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )
 I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )
I2在KI溶液中存在下列平衡:I2(aq)+I-(aq)?I3-(aq)某I2、KI混合溶液中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上任何一点都表示平衡状态,忽略I2 的挥发).下列说法正确的是( )| A. | 反应 I2(aq)+I-(aq)?I3-(aq)△H>0 | |
| B. | 状态A与状态B相比,状态A的c(I2)大 | |
| C. | 若反应进行到状态D时,一定有v逆>v正 | |
| D. | 若温度为T1、T2,反应的平衡常数K1、K2则 K1>K2 |
18.为了确认电解质溶液中部分离子相互间能否发生反应,及离子反应发生的条件,做如表四组实验.
(1)实验Ⅰ的现象有白色沉淀产生,写出反应的离子方程式Ba++SO42+=BaSO4↓.
(2)实验Ⅱ的目的是验证Cl-与Cu2+不发生反应.
(3)实验Ⅲ的现象证明了溶液中的H+、OH-两种离子之间发生了化学反应.
(4)实验Ⅳ中发生反应的离子方程式是CaCO3+2H+═Ca2++CO2↑+H2O.
0 160386 160394 160400 160404 160410 160412 160416 160422 160424 160430 160436 160440 160442 160446 160452 160454 160460 160464 160466 160470 160472 160476 160478 160480 160481 160482 160484 160485 160486 160488 160490 160494 160496 160500 160502 160506 160512 160514 160520 160524 160526 160530 160536 160542 160544 160550 160554 160556 160562 160566 160572 160580 203614
| 编号 | Ⅰ | Ⅱ | Ⅲ | Ⅳ |
| 实验 |  | 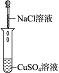 | 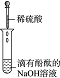 | 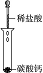 |
(2)实验Ⅱ的目的是验证Cl-与Cu2+不发生反应.
(3)实验Ⅲ的现象证明了溶液中的H+、OH-两种离子之间发生了化学反应.
(4)实验Ⅳ中发生反应的离子方程式是CaCO3+2H+═Ca2++CO2↑+H2O.