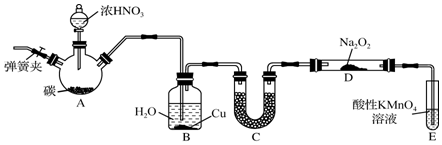
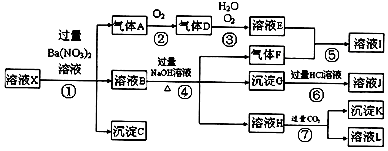
3.针对下面10种元素,完成以下各小题.
(1)地壳中含量最多的元素是氧(或氧元素)(填名称).
(2)最高价氧化物对应的水化物碱性最强的是NaOH(填化学式).
(3)Al的原子结构示意图为 .
.
(4)S和Cl相比,元素非金属性较强的是Cl.
(5)可用来制造光导纤维的物质是二氧化硅(或SiO2),晶体硅的主要用途是制造半导体材料(写出一种).
(6)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
| 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | C | N | O | Ne | ||||
| 3 | Na | Mg | Al | Si | S | Cl |
(2)最高价氧化物对应的水化物碱性最强的是NaOH(填化学式).
(3)Al的原子结构示意图为
 .
.(4)S和Cl相比,元素非金属性较强的是Cl.
(5)可用来制造光导纤维的物质是二氧化硅(或SiO2),晶体硅的主要用途是制造半导体材料(写出一种).
(6)工业上以N2和H2为原料,在高温、高压和催化剂存在的条件下制备NH3,请写出反应的化学方程式:N2+3H2$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3.
2.运用科学发展观,创建和谐社会,保护生存环境是每个公民的责任和义务.下列行为不符合社会发展与自然环境之间和谐的是( )
| A. | 推广垃圾分类投放、分类回收、分类处理 | |
| B. | 氮、磷的植物的营养元素,含氮、磷化合物的生活污水直接排放 | |
| C. | 使用沼气、太阳能、风能等能源代替传统的煤炭 | |
| D. | 研制开发燃料电池汽车,减少机动车尾气污染 |
19.X、T、Y、Z为1-36号元素,且原子序数依次增大,四种元素的性质或结构信息如表.请根据信息回答下列问题.
(1)写出元素T的离子结构示意图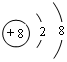 ;写出元素X的气态氢化物的电子式
;写出元素X的气态氢化物的电子式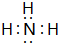 ;X形成的单质分子,含1个σ键,2个π键.写出Z元素原子的外围电子排布式3d104s1;元素Y的原子核外共有2种形状不同的电子云.
;X形成的单质分子,含1个σ键,2个π键.写出Z元素原子的外围电子排布式3d104s1;元素Y的原子核外共有2种形状不同的电子云.
(2)Y单质与氢氧化钠溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)元素T与氟元素相比,非金属性较强的是F(用元素符号表示),下列表述中能证明这一事实的是bc(填序号字母).
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目.
| 元素 | T | X | Y | Z |
| 性质结构信息 | 原子核外s电子总数等于p电子总数;人体内含量最多的元素,且其单质是常见的助燃剂 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质性质稳定,但其原子较活泼 | 第3周期元素的简单离子中半径最小 | 第4周期元素,M电子层为全充满状态,最外层只有一个电子的原子 |
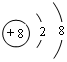 ;写出元素X的气态氢化物的电子式
;写出元素X的气态氢化物的电子式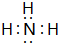 ;X形成的单质分子,含1个σ键,2个π键.写出Z元素原子的外围电子排布式3d104s1;元素Y的原子核外共有2种形状不同的电子云.
;X形成的单质分子,含1个σ键,2个π键.写出Z元素原子的外围电子排布式3d104s1;元素Y的原子核外共有2种形状不同的电子云.(2)Y单质与氢氧化钠溶液反应的离子方程式:2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)元素T与氟元素相比,非金属性较强的是F(用元素符号表示),下列表述中能证明这一事实的是bc(填序号字母).
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目.
18.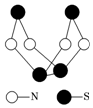 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
 现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一.其中如图是已经合成的最著名的硫-氮化合物的分子结构.下列说法正确的是( )| A. | 该物质的分子式为SN | |
| B. | 该物质的分子中只含共价键 | |
| C. | 该物质具有很高的熔、沸点 | |
| D. | 该物质与化合物S2N2互为同素异形体 |
17.下列数据是对应物质的熔点表,有关的判断正确的是( )
| Na2O | Na | AlF3 | AlCl3 | Al2O3 | BCl3 | CO2 | SiO2 |
| 920℃ | 97.8℃ | 1 291℃ | 190℃ | 2 073℃ | -107℃ | -57℃ | 1 723℃ |
| A. | 只要由金属元素和非金属元素形成的晶体就一定是离子晶体 | |
| B. | 在共价化合物分子中各原子都形成8个电子的稳定结构 | |
| C. | 金属晶体的熔点不一定比分子晶体的高 | |
| D. | 同族元素的氧化物不可能形成不同类型的晶体 |
14.X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如图所示:
请回答下列问题:
(1)W元素在周期表中的位置第三周期第VIIA族.
(2)X、Y、Z、W分别形成的简单离子的半径由小到大的顺序为O2-<N3-<Cl-<S2-(用化学式填写,下同);Y、Z对应的气态氢化物的稳定性H2O>H2S.
(3)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式为2SO2(g)+O2(g)?2SO3(g)△H=-190.0kJ•mol-1.
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O=SO2+3S+4HCl.
0 160368 160376 160382 160386 160392 160394 160398 160404 160406 160412 160418 160422 160424 160428 160434 160436 160442 160446 160448 160452 160454 160458 160460 160462 160463 160464 160466 160467 160468 160470 160472 160476 160478 160482 160484 160488 160494 160496 160502 160506 160508 160512 160518 160524 160526 160532 160536 160538 160544 160548 160554 160562 203614
| X | Y | |
| Z | W |
(1)W元素在周期表中的位置第三周期第VIIA族.
(2)X、Y、Z、W分别形成的简单离子的半径由小到大的顺序为O2-<N3-<Cl-<S2-(用化学式填写,下同);Y、Z对应的气态氢化物的稳定性H2O>H2S.
(3)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡时有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式为2SO2(g)+O2(g)?2SO3(g)△H=-190.0kJ•mol-1.
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式2S2Cl2+2H2O=SO2+3S+4HCl.
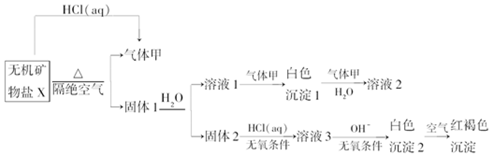
 ,写出气体甲的电子式
,写出气体甲的电子式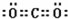 .
. 图为元素X的前五级电离能的数值示意图.已知X的原子序数小于20,请写出X基态原子核外电子的轨道表示式
图为元素X的前五级电离能的数值示意图.已知X的原子序数小于20,请写出X基态原子核外电子的轨道表示式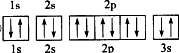 .
.