8.136C-NMR(核磁共振)可以用于含碳化合物的结构分析,请分析136C的碳原子( )
| A. | 核内有6个质子,核外有13个电子 | |
| B. | 核内有6个质子,核外有7个电子 | |
| C. | 质量数为13,原子序数为6,核内有7个质子 | |
| D. | 质量数为13,原子序数为6,核内有7个中子 |
7.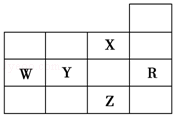 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
 如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )
如图为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )| A. | W元素的电负性大于Y元素的电负性 | |
| B. | X元素是电负性最大的元素 | |
| C. | p能级未成对电子最多的是Z元素 | |
| D. | Y、Z的阴离子电子层结构都与R原子的相同 |
6.关于小苏打水溶液的表述正确的是( )
| A. | 存在的电离平衡为:HCO3-+H2O?H2CO3+OH- | |
| B. | c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| C. | c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| D. | HCO3-的电离程度大于HCO3-的水解程度 |
5.25℃时,下列两溶液混合后所得溶液pH>7的是( )
| A. | 0.1mol/L的盐酸和0.1mol/L的氨水等体积混合 | |
| B. | pH=3的盐酸和pH=11的氢氧化钡溶液等体积混合 | |
| C. | pH=3的醋酸和pH=11的氢氧化钡溶液等体积混合 | |
| D. | pH=3的硫酸和pH=11的氨水等体积混合 |
4.在恒温恒容的密闭容器中反应:aA(g)?bB(g)+cC(g)达到化学平衡后,再充入一定量的A物质,重新达到平衡时,下列判断正确的是( )
| A. | 若a=b+c时,B的物质的量分数变大 | B. | 若a=b+c时,B的物质的量分数变小 | ||
| C. | 若a>b+c时,A的转化率不变 | D. | 若a<b+c时,A的转化率变小 |
2.下列变化中,属于还原反应的是( )
| A. | KMnO4→MnO2 | B. | FeCl2→FeCl3 | C. | C→CO2 | D. | Cl-→Cl2 |
1.设NA为阿伏加德罗常数的值,下列说法中,正确的是( )
0 160328 160336 160342 160346 160352 160354 160358 160364 160366 160372 160378 160382 160384 160388 160394 160396 160402 160406 160408 160412 160414 160418 160420 160422 160423 160424 160426 160427 160428 160430 160432 160436 160438 160442 160444 160448 160454 160456 160462 160466 160468 160472 160478 160484 160486 160492 160496 160498 160504 160508 160514 160522 203614
| A. | 2L0.5mol/L Na2SO4溶液中含NA个Na+ | |
| B. | 在常温常压下,1molHe含有的原子数为2NA | |
| C. | 2gH2所含原子数为NA | |
| D. | 在常温常压下,11.2L氮气含有的分子数小于0.5NA |
 .
.