19.向四支试管中分别加入少量不同的无色溶液进行如下操作,现象和结论正确的是( )
| 操作 | 现象 | 结论 | |
| A | 先滴加BaCl2溶液再滴加HCl溶液 | 生成白色沉淀 | 原溶液中有SO42- |
| B | 先滴加稀盐酸再滴加AgNO3溶液 | 生成白色沉淀 | 原溶液中有Cl- |
| C | 用洁净铁丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有K+ |
| D | 滴加NaOH溶液加热,将湿润红色石蕊试纸置于试管口 | 试纸变蓝 | 原溶液中有NH4+ |
| A. | A | B. | B | C. | C | D. | D |
15.NA代表阿伏加德罗常数,下列叙述错误的是( )
| A. | 在0℃,101 kPa时,22.4 L氢气中含有NA个氢原子 | |
| B. | 在H2O2+Cl2═2HCl+O2反应中,每生成32g氧气,则转移2NA个电子 | |
| C. | 标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g | |
| D. | NA个一氧化碳分子和0.5mol甲烷的质量比为7:2 |
14.一定条件下的可逆反应2SO2+O2?2SO3,下列判断能说明达到化学反应的限度的是( )
| A. | SO2完全转化为SO3 | |
| B. | SO2、O2与SO3的物质的量之比为2:1:2 | |
| C. | 反应混合物中,SO3的质量分数不再改变 | |
| D. | 消耗2 mol SO2的同时生成2 mol SO3 |
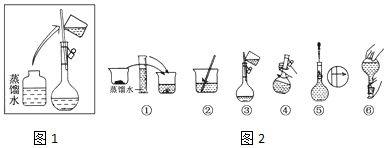
13. 用中和滴定法测定某盐酸的物质的量浓度.
用中和滴定法测定某盐酸的物质的量浓度.
(1)标准溶液应盛于A(填“A”或“B”)滴定管中.
(2)若选用酚酞作指示剂,以0.125 0mol•L-1的标准氢氧化钠溶液滴定,如何判断滴定终点当加入最后一滴标准液时,溶液恰好出现红色且半分钟内红色不褪去
(3)实验数据记录如表,请分析数据并计算,盐酸的物质的量浓度=0.1250mol•L-1
0 160323 160331 160337 160341 160347 160349 160353 160359 160361 160367 160373 160377 160379 160383 160389 160391 160397 160401 160403 160407 160409 160413 160415 160417 160418 160419 160421 160422 160423 160425 160427 160431 160433 160437 160439 160443 160449 160451 160457 160461 160463 160467 160473 160479 160481 160487 160491 160493 160499 160503 160509 160517 203614
 用中和滴定法测定某盐酸的物质的量浓度.
用中和滴定法测定某盐酸的物质的量浓度.(1)标准溶液应盛于A(填“A”或“B”)滴定管中.
(2)若选用酚酞作指示剂,以0.125 0mol•L-1的标准氢氧化钠溶液滴定,如何判断滴定终点当加入最后一滴标准液时,溶液恰好出现红色且半分钟内红色不褪去
(3)实验数据记录如表,请分析数据并计算,盐酸的物质的量浓度=0.1250mol•L-1
| 滴定次数 | 待测液体体积/mL | 标准碱液 | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| ① | 20.0 | 0.40 | 20.41 |
| ② | 20.0 | 0.10 | 20.60 |
| ③ | 20.0 | 4.00 | 23.99 |

 ;I
;I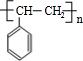 .
. ;
; +NaOH$→_{△}^{H_{2}O}$
+NaOH$→_{△}^{H_{2}O}$ +NaCl;
+NaCl; 或
或 .
.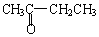
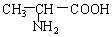 与
与
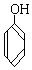 与
与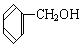
 与
与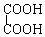
 (写结构简式).
(写结构简式).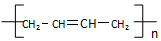 .
.