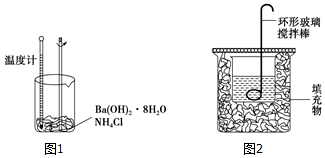
12.(1)砷原子核外电子排布式为1s22s22p63s23p63d104s24p3.
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道).
(3)H2S和H2O2的主要物理性质比较如表:
H2S和H2O2的相对分子质量基本相同,造成上述物理性质差异的主要原因H2O2分子之间会形成氢键,所以熔沸点高,H2O2与水分子之间会形成氢键,所以溶解度大.
(4)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、范德华力.
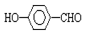 的沸点比
的沸点比 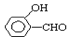 高,原因是:
高,原因是: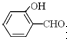 形成分子内氢键,而
形成分子内氢键,而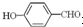 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.
(5)H+可与H2O形成H3O+,H3O+中O原子采用sp3杂化.H3O+中H-O-H键角比H2O中H-O-H键角大,原因为H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,排斥力较小.
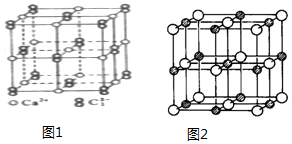
(6)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为ag•cm-3,NA表示阿伏加德罗常数,则CaO晶胞体积为$\frac{224}{a{N}_{A}}$cm3.
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为配位键,该化学键能够形成的原因是CN-能提供孤对电子,Fe3+能接受孤对电子(或Fe3+有空轨道).
(3)H2S和H2O2的主要物理性质比较如表:
| 熔点/K | 沸点/K | 标准状况时在水中的溶解度 | |
| H2S | 187 | 202 | 2.6 |
| H2O2 | 272 | 423 | 以任意比互溶 |
(4)H2O分子内的O-H键、分子间的范德华力和氢键从强到弱依次为O-H键、氢键、范德华力.
 的沸点比
的沸点比  高,原因是:
高,原因是: 形成分子内氢键,而
形成分子内氢键,而 形成分子间氢键,分子间氢键使分子间作用力增大.
形成分子间氢键,分子间氢键使分子间作用力增大.(5)H+可与H2O形成H3O+,H3O+中O原子采用sp3杂化.H3O+中H-O-H键角比H2O中H-O-H键角大,原因为H2O中O原子有两对孤对电子,H3O+中O原子有一对孤对电子,排斥力较小.
(6)CaO与NaCl的晶胞同为面心立方结构,已知CaO晶体密度为ag•cm-3,NA表示阿伏加德罗常数,则CaO晶胞体积为$\frac{224}{a{N}_{A}}$cm3.
9. 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示:
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示:
(1)上述反应平衡常数K的表达式为$\frac{c({H}_{2}O)c(C{H}_{3}OH)}{{c}^{3}({H}_{2})c(C{O}_{2})}$,温度降低,平衡常数K增大(填“增大”、“不变”或“减小”).
(2)在体积为2L的密闭容器中,充入1mol CO2和3mol H2,测得CO2的物质的量随时间变化如表所示.从反应开始到5min末,用CO2浓度变化表示的平均反应速率v(CO2)=0.05mol/(L•min).
(3)下列条件能使上述反应的反应速率增大,且平衡向正反应方向移动的是C(填写序号字母)
A.及时分离出CH3OH气体 B.适当升高温度
C.保持容器的容积不变,再充入1mol CO2和3mol H2D.选择高效催化剂.
0 160303 160311 160317 160321 160327 160329 160333 160339 160341 160347 160353 160357 160359 160363 160369 160371 160377 160381 160383 160387 160389 160393 160395 160397 160398 160399 160401 160402 160403 160405 160407 160411 160413 160417 160419 160423 160429 160431 160437 160441 160443 160447 160453 160459 160461 160467 160471 160473 160479 160483 160489 160497 203614
 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示:
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引用了各界的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示:(1)上述反应平衡常数K的表达式为$\frac{c({H}_{2}O)c(C{H}_{3}OH)}{{c}^{3}({H}_{2})c(C{O}_{2})}$,温度降低,平衡常数K增大(填“增大”、“不变”或“减小”).
(2)在体积为2L的密闭容器中,充入1mol CO2和3mol H2,测得CO2的物质的量随时间变化如表所示.从反应开始到5min末,用CO2浓度变化表示的平均反应速率v(CO2)=0.05mol/(L•min).
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
A.及时分离出CH3OH气体 B.适当升高温度
C.保持容器的容积不变,再充入1mol CO2和3mol H2D.选择高效催化剂.

 实验室常用以下方法制取氯气:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O,氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答
实验室常用以下方法制取氯气:MnO2+4HCl(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ MnCl2+Cl2↑+2H2O,氯气是一种重要的化工原料,在工农业生产、生活中有着重要的应用.请你根据所学知识回答
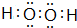 .
.
 .
.