12.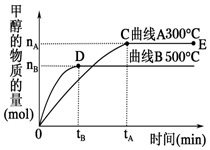 一定条件下,在容积为3L的密闭容器中,发生反应CO(g)+2H2(g)?CH3OH(g)△H<0,在不同温度下甲醇的物质的量随时间的变化如图所示.下列叙述正确的是( )
一定条件下,在容积为3L的密闭容器中,发生反应CO(g)+2H2(g)?CH3OH(g)△H<0,在不同温度下甲醇的物质的量随时间的变化如图所示.下列叙述正确的是( )
 一定条件下,在容积为3L的密闭容器中,发生反应CO(g)+2H2(g)?CH3OH(g)△H<0,在不同温度下甲醇的物质的量随时间的变化如图所示.下列叙述正确的是( )
一定条件下,在容积为3L的密闭容器中,发生反应CO(g)+2H2(g)?CH3OH(g)△H<0,在不同温度下甲醇的物质的量随时间的变化如图所示.下列叙述正确的是( )| A. | 平衡常数K(300℃)<K(500℃) | |
| B. | 500℃,从反应开始到平衡,氢气的平均反应速率v(H2)=$\frac{nB}{3tB}$ mol•L-1•min-1 | |
| C. | 在其他条件不变的情况下,将处于E点的体系的容积压缩到原来的$\frac{1}{2}$,氢气的浓度减小 | |
| D. | 300℃,当容器内压强不变时说明反应已经达到平衡 |
11.已知:2C(s)+O2(g)═2CO(g)△H=-Q1 kJ•mol-1;
C(s)+O2(g)═CO2(g)△H=-Q2 kJ•mol-1;
S(s)+O2(g)═SO2(g)△H=-Q3 kJ•mol-1.
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为( )
C(s)+O2(g)═CO2(g)△H=-Q2 kJ•mol-1;
S(s)+O2(g)═SO2(g)△H=-Q3 kJ•mol-1.
CO与镍反应会造成镍催化剂中毒,为防止镍催化剂中毒,工业上常用SO2将CO氧化,二氧化硫转化为单质硫,则该反应的热化学方程式为( )
| A. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-2Q2+Q3) kJ•mol-1 | |
| B. | S(s)+2CO(g)═SO2(g)+2C(s)△H=(Q1-Q3) kJ•mol-1 | |
| C. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(Q1-2Q2+Q3) kJ•mol-1 | |
| D. | SO2(g)+2CO(g)═S(s)+2CO2(g)△H=(2Q1-Q2+2Q3) kJ•mol-1 |
10.下列说法正确的是( )
| A. | 需要加热才能发生的反应一定是吸热反应 | |
| B. | △H>0表示产物的总能量低于反应物的总能量 | |
| C. | △H 的单位kJ•mol-1,热量Q的单位为kJ | |
| D. | 化学键断裂过程中释放能量 |
9.下列各组能源中,前者是化石能源,后者是新能源的是( )
| A. | 氢气、天然气 | B. | 液化气、核能 | C. | 太阳能、风能 | D. | 燃煤、97#汽油 |
8.乙酸乙酯在KOH溶液催化下水解得到的产物是( )
| A. | 乙酸和乙醇 | B. | 甲酸和乙醇 | C. | 乙酸钾和乙醇 | D. | 乙酸和甲醇 |
6.甲、乙、丙、丁四种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成.已知:①将甲溶液分别与其它三种物质的溶液混合,均有白色沉淀生成;②0.1mol•L-1乙溶液中c(H+)>0.1mol•L-1;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成.下列结论不正确的是( )
| A. | 甲溶液含有OH- | B. | 乙溶液含有SO42- | C. | 丙溶液含有Cl- | D. | 丁溶液含有Mg2+ |
5.下列关于分散系的叙述中错误的是( )
0 160285 160293 160299 160303 160309 160311 160315 160321 160323 160329 160335 160339 160341 160345 160351 160353 160359 160363 160365 160369 160371 160375 160377 160379 160380 160381 160383 160384 160385 160387 160389 160393 160395 160399 160401 160405 160411 160413 160419 160423 160425 160429 160435 160441 160443 160449 160453 160455 160461 160465 160471 160479 203614
| A. | 当光束通过下列分散系:有尘埃的空气、豆浆、墨水都能观察到丁达尔效应 | |
| B. | 溶液、胶体、浊液的根本区别是分散质微粒直径的大小 | |
| C. | 把1mL0.1mol/L三氯化铁溶液滴加入20mL沸水中,边加边振荡,可制得氢氧化铁胶体 | |
| D. | 胶体的稳定性介于溶液和浊液之间,属于介稳体系 |
