16.已知A(g)+B(g)?C(g)+D(s)反应的平衡常数与温度的关系如下:
(1)该反应的平衡常数表达式K=$\frac{c(C)}{c(A)c(B)}$,△H>0(填“>、<、或=”);
(2)800℃时,向一个5L的密闭容器中充入0.4molA和0.7molB,若反应初始2mim内A的平均反应速率为0.01mol•L-1•min-1,则2min时c(A)=0.06mol•L-1,C的物质的量为0.1mol;此时,该可逆反应是否达到平衡?否(填“是”或“否”)
(3)在此密闭容器中,下列选项能作为判断该反应达到平衡的依据有abd
a.压强不随时间改变 b.气体的密度不随时间改变
c.单位时间内消耗A和B的物质的量相等 d.C的百分含量保持不变
(4)880℃时,反应 C(g)+D(s)?A(g)+B(g)的平衡常数的值为0.067.
| 温度℃ | 700 | 800 | 880 | 1000 | 1200 |
| 平衡常数 | 1.0 | 10.0 | 15.0 | 16.1 | 17.7 |
(2)800℃时,向一个5L的密闭容器中充入0.4molA和0.7molB,若反应初始2mim内A的平均反应速率为0.01mol•L-1•min-1,则2min时c(A)=0.06mol•L-1,C的物质的量为0.1mol;此时,该可逆反应是否达到平衡?否(填“是”或“否”)
(3)在此密闭容器中,下列选项能作为判断该反应达到平衡的依据有abd
a.压强不随时间改变 b.气体的密度不随时间改变
c.单位时间内消耗A和B的物质的量相等 d.C的百分含量保持不变
(4)880℃时,反应 C(g)+D(s)?A(g)+B(g)的平衡常数的值为0.067.
15.CH4是一种重要的化石燃料,在工农业生产中有着极其重要的应用.用甲烷可以消除氮氧化物的污染,其反应如下:
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g).
在130℃和180℃时,分别将0.50mol CH4和a mol NO2充入1L的密闭容器中发生反应,测得有关数据如表:
(1)130℃时,达到平衡状态时CH4的转化率为80%.当温度为180℃、反应到40min时,该反应是(填“是”或“否”)达到平衡,推断的依据是温度升高,反应加快,对比实验1,高温下比低温下更快达到平衡状态.
(2)由表中数据分析可知,该反应的△H<0(填“=”、“>”或“<”),130℃和180℃平衡常数的关系:K(130℃)>K(180℃)(填“=”、“>”或“<”).
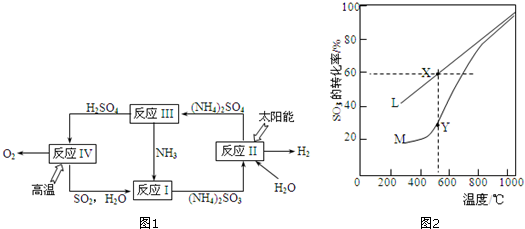
(3)如图1所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜.
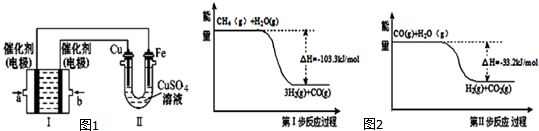
①a电极上发生反应的电极反应式是CH4+10OH--8e-=CO32-+7H2O.
②电镀结束后,装置Ⅰ中溶液的pH减小(填“增大”、“减小”或“不变”).
③若完全反应后,装置Ⅱ中Cu极质量减少12.8g,则装置Ⅰ中理论上消耗甲烷1.12L(标准状况下).
(4)用甲烷制取氢气的反应分为两步,其能量变化如图2所示:
写出甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5 kJ/mol.
CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(g).
在130℃和180℃时,分别将0.50mol CH4和a mol NO2充入1L的密闭容器中发生反应,测得有关数据如表:
| 实验编号 | 温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
(2)由表中数据分析可知,该反应的△H<0(填“=”、“>”或“<”),130℃和180℃平衡常数的关系:K(130℃)>K(180℃)(填“=”、“>”或“<”).
(3)如图1所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH溶液),通过装置Ⅱ实现铁棒上镀铜.

①a电极上发生反应的电极反应式是CH4+10OH--8e-=CO32-+7H2O.
②电镀结束后,装置Ⅰ中溶液的pH减小(填“增大”、“减小”或“不变”).
③若完全反应后,装置Ⅱ中Cu极质量减少12.8g,则装置Ⅰ中理论上消耗甲烷1.12L(标准状况下).
(4)用甲烷制取氢气的反应分为两步,其能量变化如图2所示:
写出甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式CH4(g)+2H2O(g)=4H2(g)+CO2(g)△H=-136.5 kJ/mol.
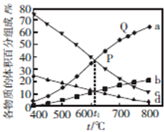
13. 一定条件下存在反应C(s)+H2O(g)?C O(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示.则下列说法正确的是( )
一定条件下存在反应C(s)+H2O(g)?C O(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示.则下列说法正确的是( )
 一定条件下存在反应C(s)+H2O(g)?C O(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示.则下列说法正确的是( )
一定条件下存在反应C(s)+H2O(g)?C O(g)+H2(g):向甲、乙、丙三个恒容容器中加入一定量C和H2O,各容器中温度、反应物的起始量如表,反应过程中CO的物质的量浓度随时间变化如图所示.则下列说法正确的是( )| 容 器 | 甲 | 乙 | 丙 |
| 容 积 | 0.5L | 0.5L | V |
| 温 度 | T1℃ | T2℃ | T1℃ |
| 起始量 | 2molC 1molH2O | 1molCO 1molH2 | 4molC 2molH2O |
| A. | 甲容器中,反应在前15min的平均速率v(H2)=0.2mol•L-1•min-1 | |
| B. | 丙容器的体积V>0.5L | |
| C. | 当温度为T1℃时,反应的平衡常数K=4.5(mol•L-1) | |
| D. | 乙容器中,若平衡时n(H2O)=0.4mol,则T1<T2 |
12. 中国是世界上第一钢铁生产大国,近两年钢铁行业形式急转直下,不少钢铁企业陷入全面亏损,2015年,钢铁年产量出现34年来的首次下降.原因就是因为高炉炼铁技术低级落后,不能生产高附加值产品.请根据所学知识回答下列问题:
中国是世界上第一钢铁生产大国,近两年钢铁行业形式急转直下,不少钢铁企业陷入全面亏损,2015年,钢铁年产量出现34年来的首次下降.原因就是因为高炉炼铁技术低级落后,不能生产高附加值产品.请根据所学知识回答下列问题:
(1)地壳中含量最多的金属元素的单质与氧化铁在高温下发生反应可用于焊接钢轨,该反应的化学方程式为2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(2)CO(g)+FeO(s)=CO2(g)+Fe(s)△H=-218.03kJ•mol-1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ•mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
则反应Fe2O3(s)+3CO(g)?2Fe (s)+3CO2(g)的△H=-24.8kJ•mol-1.
(3)在T℃、2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
①反应达到平衡后,再通入一定量的氩气,则CO的转化率将不变(填“增大”、“减小”、“不变”);
②若甲容器中CO的平衡转化率为60%,则T℃时,反应Fe2O3(s)+3CO(g)?2Fe (s)+3CO2(g)的平衡常数K=64;
③下列说法正确的是B
A.若容器压强恒定,反应达到平衡状态
B.若容器内混合气体密度恒定,反应达到平衡状态
C.甲、乙容器中CO的平衡转化率相等
D.增加Fe2O3粉末的物质的量就能提高CO的转化率
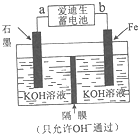
(4)铁与金属镍在碱性条件下可形成二次电池,俗称爱迪生蓄电池.利用爱迪生蓄电池可以制取少量高锰酸钾(装置如图所示),此装置中负极是a(填“a”或“b”),写出阳极的电极反应式Fe-6e-+8OH-=FeO42-+4H2O;当生成19.8g的K2FeO4时,电路中转移的电子的物质的量为0.6mol.
 中国是世界上第一钢铁生产大国,近两年钢铁行业形式急转直下,不少钢铁企业陷入全面亏损,2015年,钢铁年产量出现34年来的首次下降.原因就是因为高炉炼铁技术低级落后,不能生产高附加值产品.请根据所学知识回答下列问题:
中国是世界上第一钢铁生产大国,近两年钢铁行业形式急转直下,不少钢铁企业陷入全面亏损,2015年,钢铁年产量出现34年来的首次下降.原因就是因为高炉炼铁技术低级落后,不能生产高附加值产品.请根据所学知识回答下列问题:(1)地壳中含量最多的金属元素的单质与氧化铁在高温下发生反应可用于焊接钢轨,该反应的化学方程式为2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3;
(2)CO(g)+FeO(s)=CO2(g)+Fe(s)△H=-218.03kJ•mol-1
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g)△H=-47.2kJ•mol-1
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g)△H=+640.5kJ•mol-1
则反应Fe2O3(s)+3CO(g)?2Fe (s)+3CO2(g)的△H=-24.8kJ•mol-1.
(3)在T℃、2L恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡.
| Fe2O3 | CO | Fe | CO2 | |
| 甲/mol | 1.0 | 1.0 | 1.0 | 1.0 |
| 乙/mol | 1.0 | 1.5 | 1.0 | 1.0 |
②若甲容器中CO的平衡转化率为60%,则T℃时,反应Fe2O3(s)+3CO(g)?2Fe (s)+3CO2(g)的平衡常数K=64;
③下列说法正确的是B
A.若容器压强恒定,反应达到平衡状态
B.若容器内混合气体密度恒定,反应达到平衡状态
C.甲、乙容器中CO的平衡转化率相等
D.增加Fe2O3粉末的物质的量就能提高CO的转化率
(4)铁与金属镍在碱性条件下可形成二次电池,俗称爱迪生蓄电池.利用爱迪生蓄电池可以制取少量高锰酸钾(装置如图所示),此装置中负极是a(填“a”或“b”),写出阳极的电极反应式Fe-6e-+8OH-=FeO42-+4H2O;当生成19.8g的K2FeO4时,电路中转移的电子的物质的量为0.6mol.
9.T℃时,在容积为2L的3个恒容密闭容器中发生反应:3A(g)+B(g)?xC(g),按不同方式投入反应物,测得反应达到平衡时的有关数据如下:
下列说法正确的是( )
0 160259 160267 160273 160277 160283 160285 160289 160295 160297 160303 160309 160313 160315 160319 160325 160327 160333 160337 160339 160343 160345 160349 160351 160353 160354 160355 160357 160358 160359 160361 160363 160367 160369 160373 160375 160379 160385 160387 160393 160397 160399 160403 160409 160415 160417 160423 160427 160429 160435 160439 160445 160453 203614
| 容器 | 甲 | 乙 | 丙 |
| 反应物的投入量 | 3molA、2molB | 6molA、4molB | 2molC |
| 达到平衡的时间/min | 5 | 8 | |
| A的浓度/mol•L-1 | C1 | C2 | |
| C的体积分数/% | ω1 | ω3 | |
| 混合气体的密度/g•L-1 | ρ1 | ρ2 |
| A. | 若 x<4,2C1<C2 | |
| B. | 容器甲达到平衡所需的时间比容器乙达到平衡所需的时间短 | |
| C. | 无论x的值是多少,均有2ρ1=ρ2 | |
| D. | 若 x=4,则ω1=ω3 |
 郑州一中是一所具有丰厚的历史积淀、独特的精神内涵,以关注学生智慧与灵魂为学校文化内核,充满创新精神,能够培养具有国际视野的拔尖人才,拥有核心竞争力的国内名校.目前一中教育集团包含小学部、初中部、高中部三个学部的十余所学校.学校以主体课堂教学为载体,以培养学生的创新思维和实践能力为目标,在教学活动中特别注重学生科学素养的提升,如对于I A和ⅥA族重要元素化合物的性质,各校区根据实际情况开展了丰富多彩的探究活动.
郑州一中是一所具有丰厚的历史积淀、独特的精神内涵,以关注学生智慧与灵魂为学校文化内核,充满创新精神,能够培养具有国际视野的拔尖人才,拥有核心竞争力的国内名校.目前一中教育集团包含小学部、初中部、高中部三个学部的十余所学校.学校以主体课堂教学为载体,以培养学生的创新思维和实践能力为目标,在教学活动中特别注重学生科学素养的提升,如对于I A和ⅥA族重要元素化合物的性质,各校区根据实际情况开展了丰富多彩的探究活动. .
.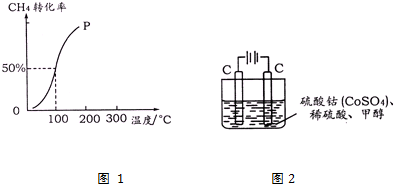

 CO2与H2合成甲醚的主要反应如下:
CO2与H2合成甲醚的主要反应如下: