9.已知常温常压下,P2和P4燃烧的热化学方程式分别为:
2P2(g)+5O2(g)═P4O10(s)△H=-2 695.4kJ•mol-1,
P4(g)+5O2(g)═P4O10(s)△H=-2 925.1kJ•mol-1.则下列说法正确的是( )
2P2(g)+5O2(g)═P4O10(s)△H=-2 695.4kJ•mol-1,
P4(g)+5O2(g)═P4O10(s)△H=-2 925.1kJ•mol-1.则下列说法正确的是( )
| A. | 2P2(g)═P4(g)△H=-229.7 kJ•mol-1 | B. | P2制P4是放热反应 | ||
| C. | P2比P4更加稳定 | D. | 等质量时,P2比P4具有的能量高 |
8.如表是周期表中的一部分,根据A-K在周期表中的位置,用元素符号或化学式回答.
(1)表中元素,化学性质最不活泼的是Ne,只有负价而无正价的是F,氧化性最强的单质是F2,还原性最强的单质是K.
(2)最高价氧化物的水化物碱性最强的是KOH,酸性最强的是HClO4,呈两性的是Al(OH)3.
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HF,
(4)在这些元素中(除I外),原子半径最大的是K,原子半径最小的是F
(5)D和K组成化合物的电子式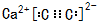 ,
,
(6)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式:Al2O3+2OH-=2AlO2-+2H2O.
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H | ||||
| 4 | J | K |
(2)最高价氧化物的水化物碱性最强的是KOH,酸性最强的是HClO4,呈两性的是Al(OH)3.
(3)A分别与D、E、F、G、H形成的化合物中,最稳定的HF,
(4)在这些元素中(除I外),原子半径最大的是K,原子半径最小的是F
(5)D和K组成化合物的电子式
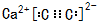 ,
,(6)B的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式:Al2O3+2OH-=2AlO2-+2H2O.
20.用图所示装置进行实验,下表中所得结论正确的是( )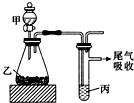
0 160244 160252 160258 160262 160268 160270 160274 160280 160282 160288 160294 160298 160300 160304 160310 160312 160318 160322 160324 160328 160330 160334 160336 160338 160339 160340 160342 160343 160344 160346 160348 160352 160354 160358 160360 160364 160370 160372 160378 160382 160384 160388 160394 160400 160402 160408 160412 160414 160420 160424 160430 160438 203614

| 甲 | 乙 | 丙 | 结论 | |
| A | 水 | 电石 | 溴水 | 稳定性:H2O>C2H2>Br2 |
| B | 盐酸 | 硫化亚铁 | 溴水 | 还原性:Cl->Br->S2- |
| C | 浓盐酸 | 高锰酸钾 | 溴化钾溶液 | 氧化性:高锰酸钾>Cl2>Br2 |
| D | 盐酸 | 石灰石 | 苯酚钠溶液 | 酸性:HCl>H2CO3>苯酚 |
| A. | A | B. | B | C. | C | D. | D |
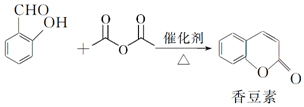
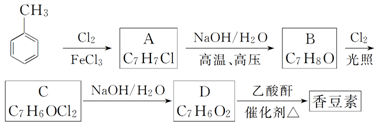
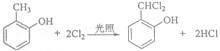 ;
;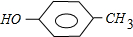 和
和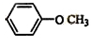 .
. 反应类型加聚反应
反应类型加聚反应 反应类型取代反应
反应类型取代反应 反应类型取代反应
反应类型取代反应
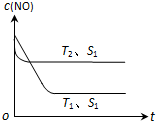 汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务.
汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务. .
.