5.电离平衡常数是衡量弱电解质电离程度强弱的量.已知如表数据.
(1)25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为Na2CO3溶液>NaCN溶液>CH3COONa溶液.
(2)25℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)>c(CH3COO-)(填“>”、“<”或“=”).
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
(4)25℃时,pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=9.9×10-7mol/L.
| 化学式 | 电离平衡常数(25℃) |
| HCN | K=4.9×10-10 |
| CH3COOH | K=1.8×10-5 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(2)25℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)>c(CH3COO-)(填“>”、“<”或“=”).
(3)NaCN溶液中通入少量CO2,所发生反应的化学方程式为NaCN+H2O+CO2=HCN+NaHCO3.
(4)25℃时,pH=8的CH3COONa溶液中,c(Na+)-c(CH3COO-)=9.9×10-7mol/L.
4.下列说法正确的是( )
| A. | 任何酸与碱发生中和反应生成1molH2O的过程中,能量变化均相同 | |
| B. | 中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 | |
| C. | 若①2H2(g)+O2(g)═2H2O(g)△H=-akJ•mol-1,②2H2(g)+O2(g)═2H2O(l)△H=-bkJ•mol-1,则 a>b | |
| D. | 能自发进行的反应一定是放热反应,不能自发进行的反应一定是吸热反应 |
3.下列表述中合理的是( )
| A. | 在101kPa下,1g物质完全燃烧所放出的热量叫做该物质的热值 | |
| B. | 把FeCl3的水溶液加热蒸干可得到FeCl3固体 | |
| C. | 用25mL碱式滴定管量取20.00mL高锰酸钾溶液 | |
| D. | 太阳能电池是把太阳能转化为内能的装置 |
2.如图所示,下列说法正确的是( )
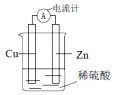

| A. | 该装置中能量转化方式为电能转化为化学能 | |
| B. | 电子从锌片流出,经导线流向铜片 | |
| C. | 工作一段时间之后,溶液颜色逐渐变蓝 | |
| D. | 锌片发生还原反应 |
1.常温下c(H+)最小的是下列各项中的( )
| A. | pH=0的溶液 | B. | 0.5mol•L-1H2SO4 | ||
| C. | 0.5mol•L-1HCl | D. | 0.5mol•L-1CH3COOH |
19.将SO2气体与足量Fe2(SO4)3溶液完全反应后,再加入K2Cr2O7溶液,发生如下两个反应:
SO2+2Fe3++2H2O═SO42-+4H++2Fe2+,
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
下列说法正确的是( )
0 160233 160241 160247 160251 160257 160259 160263 160269 160271 160277 160283 160287 160289 160293 160299 160301 160307 160311 160313 160317 160319 160323 160325 160327 160328 160329 160331 160332 160333 160335 160337 160341 160343 160347 160349 160353 160359 160361 160367 160371 160373 160377 160383 160389 160391 160397 160401 160403 160409 160413 160419 160427 203614
SO2+2Fe3++2H2O═SO42-+4H++2Fe2+,
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
下列说法正确的是( )
| A. | Cr2O72-不能将SO2氧化 | B. | 还原性:Cr3+>Fe2+>SO2 | ||
| C. | 氧化性:Cr2O72->Fe3+>SO2 | D. | 两个反应中Fe3+均表现还原性 |
 如图所示的装置,X、Y都是惰性电极.将电源接通后,向(甲)中滴入酚酞溶液此空不填,在Fe极附近显红色.丙池中盛有100mL3.00mol•L-1的CuSO4溶液.试回答下列问题:
如图所示的装置,X、Y都是惰性电极.将电源接通后,向(甲)中滴入酚酞溶液此空不填,在Fe极附近显红色.丙池中盛有100mL3.00mol•L-1的CuSO4溶液.试回答下列问题:
 ,K的结构简式为
,K的结构简式为 .
.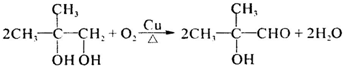 .
. $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$ +H2O.
+H2O. $→_{①}^{Cl_{2},光照}$
$→_{①}^{Cl_{2},光照}$ $→_{②}^{NaOH,乙醇,△}$A$→_{③}^{溴水}$B$\stackrel{④}{→}$
$→_{②}^{NaOH,乙醇,△}$A$→_{③}^{溴水}$B$\stackrel{④}{→}$ $→_{⑤}^{Br_{2},催化剂}$
$→_{⑤}^{Br_{2},催化剂}$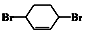 $\stackrel{⑥}{→}$
$\stackrel{⑥}{→}$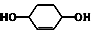
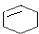 ,B的结构简式是
,B的结构简式是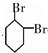 .
. .
.