2. 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
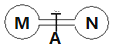
 室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )
室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压),取下弹簧夹A,使两烧瓶内的气体充分接触(如图),容器内的压强由大到小的顺序是( )| 编号 | ① | ② | ③ | ④ |
| 气体M | H2S | NH3 | HI | NO |
| 气体N | SO2 | HCl | Cl2 | O2 |
| A. | ③=④>①>② | B. | ③>④>①>② | C. | ④>③>②>① | D. | ④>③>①>② |
20.下列有关化学用语表示正确的是( )
| A. | 过氧化钠的电子式: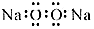 | B. | 次氯酸钠的结构式:H-Cl-OC | ||
| C. | 氯化铵的电子式: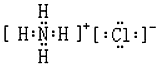 | D. | 硫离子的结构示意图: |
19.下列说法正确的是( )
| A. | HClO 中氯元素化合价比 HClO4 中氯元素化合价低,所以 HClO4 的氧化性强 | |
| B. | 已知①Fe+Cu2+═Fe2++Cu; ②2Fe3++Cu═2Fe2++Cu2+,则氧化性强弱顺序为:Fe3+>Cu2+>Fe2+ | |
| C. | 已知还原性 B->C->D-,反应 2C-+D2═2D-+C2 和 2C-+B2=2B-+C2 都能发生 | |
| D. | 具有强氧化性和强还原性的物质放在一起就能发生氧化还原反应 |
16.对已达化学平衡的反应3H2(g)+N2 (g)?2NH3(g)△H<0,降低温度对化学平衡的影响是( )
| A. | 正、逆反应速率都减小,平衡向正反应方向移动 | |
| B. | 正、逆反应速率都增大,平衡向正反应方向移动 | |
| C. | 逆反应速率増大,正反应速率减小,平衡向逆反应方向移动 | |
| D. | 逆反应速率减小,正反应速率増大,平衡向正反应方向移动 |
14.一定温度下,向aL的密闭容器中加入2molNO2(g),发生如下反应:2NO2?2NO+O2,此反应达到平衡的标志是( )
| A. | 混合气体中NO2、NO和O2的物质的量之比为2:2:1 | |
| B. | 单位时间内生成2nmolNO同时生成2nmolNO2 | |
| C. | 单位时间内生成2nmolNO同时生成nmolO2 | |
| D. | 混合气体的颜色变浅 |
13.升高温度能加快反应速率的主要原因是( )
0 160222 160230 160236 160240 160246 160248 160252 160258 160260 160266 160272 160276 160278 160282 160288 160290 160296 160300 160302 160306 160308 160312 160314 160316 160317 160318 160320 160321 160322 160324 160326 160330 160332 160336 160338 160342 160348 160350 160356 160360 160362 160366 160372 160378 160380 160386 160390 160392 160398 160402 160408 160416 203614
| A. | 活化分子的能量不变 | B. | 增加了活化分子的百分数 | ||
| C. | 降低了反应的活化能 | D. | 改变了化学反应的能量变化 |
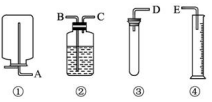 现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图
现有如下药品和装置:质量为w(w<1g)的锌片、稀H2SO4、无水硫酸铜和蒸馏水,设计一个简单实验,测定Zn的相对原子质量(气体体积均可认为是在标准状况下测定)如图 如图中的两条线分别代表的是:1g C3H6和1g M气体在相同容积的容器中,测得容器中的压强和温度的关系,试根据图形判断M气体的相对分子质量为( )
如图中的两条线分别代表的是:1g C3H6和1g M气体在相同容积的容器中,测得容器中的压强和温度的关系,试根据图形判断M气体的相对分子质量为( )